题目内容
【题目】在学习酸的化学性质后,同学们做了如图所示的A、B两个实验: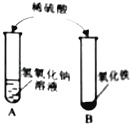
(1)A试管中发生反应的化学方程式 . 向B试管中的加入足量的稀硫酸,观察到的现象是 .
(2)实验结束后,小红将A、B两试管中的废液倒入同一洁净的烧杯中,片刻后发现烧杯中出现了红褐色沉淀,经分析,红褐色沉淀是氢氧化铁.
小红将烧杯中物质进行过滤得到无色滤液,滤液中含有什么溶质?小红、小军对此进行探究.
【实验讨论】
①小红分析了反应物和生成物之后,认为滤液中不可能有H2SO4 , 因为 .
②小军认为滤液中不可能有Fe2(SO4)3 , 理由是 .
(3)【提出猜想】
猜想Ⅰ:Na2SO4 NaOH
猜想Ⅱ:
(4)【设计实验】
实验操作 | 实验现象 | 结论 |
取少量滤液于试管中,向其中滴加酚酞试液 | 猜想Ⅰ成立 |
【答案】
(1)2NaOH+H2SO4═Na2SO4+2H2O;红棕色固体逐渐溶解至消失,溶液由无色变为黄色
(2)烧杯中生成的氢氧化铁沉淀不能与稀硫酸共存;过滤得到无色滤液,而Fe2(SO4)3溶液是黄色溶液
(3)Na2SO4
(4)酚酞试液由无色变为红色
【解析】(1)A试管中稀硫酸与氢氧化钠溶液反应生成硫酸钠和水,反应的化学方程式为:2NaOH+H2SO4═Na2SO4+2H2O.向B试管中的加入足量的稀硫酸,氧化铁与稀硫酸反应生成硫酸铁和水,观察到的现象是红棕色固体逐渐溶解至消失,溶液由无色变为黄色.(2)【实验讨论】①根据实验现象,生成了氢氧化铁沉淀,氢氧化铁沉淀能与稀硫酸反应,故小红分析了反应物和生成物之后,认为滤液中不可能有H2SO4 , 原因是烧杯中生成的氢氧化铁沉淀不能与稀硫酸共存.②烧杯中物质进行过滤得到无色滤液,Fe2(SO4)3溶液是黄色溶液,故小军认为滤液中不可能有Fe2(SO4)3 .
【提出猜想】氢氧化钠与B试管中的硫酸铁溶液反应生成氢氧化铁沉淀和硫酸钠,由于过滤得到无色滤液,不可能存在硫酸铁,但可能存在氢氧化钠,故猜想Ⅰ是Na2SO4、NaOH;也可能是恰好完全反应,故猜想Ⅱ:是Na2SO4 .
【设计实验】设计实验证明是否存在氢氧化钠即可,氢氧化钠溶液显碱性,由实验结论猜想Ⅰ成立,则取少量滤液于试管中,向其中滴加酚酞试液,酚酞试液变红色.
所以答案是:(1)2NaOH+H2SO4═Na2SO4+2H2O;红棕色固体逐渐溶解至消失,溶液由无色变为黄色;(2)【实验讨论】①烧杯中生成的氢氧化铁沉淀不能与稀硫酸共存;②过滤得到无色滤液,而Fe2(SO4)3溶液是黄色溶液.
【提出猜想】Na2SO4;
【设计实验】
实验操作 | 实验现象 | 结论 |
取少量滤液于试管中,向其中滴加酚酞试液 | 酚酞试液由无色变为红色 | 猜想Ⅰ成立 |
【考点精析】解答此题的关键在于理解书写化学方程式、文字表达式、电离方程式的相关知识,掌握注意:a、配平 b、条件 c、箭号.

 高中必刷题系列答案
高中必刷题系列答案【题目】小芳同学采用如下方法测定石灰石中碳酸钙的质量分数:取该石灰石样品10g,把40g稀盐酸分四次加入,实验过程所得数据如表(石灰石样品中含有的二氧化硅等杂质不溶于水也不与稀盐酸反应)
实验次数 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
1 | 10 | 7.5 |
2 | 10 | 5.0 |
3 | 10 | 3.2 |
4 | 10 | a |
根据实验数据计算:
(1)表中a的数值为;
(2)样品中碳酸钙的质量分数是;
(3)求盐酸中溶质的质量分数.