题目内容
【题目】小芳同学采用如下方法测定石灰石中碳酸钙的质量分数:取该石灰石样品10g,把40g稀盐酸分四次加入,实验过程所得数据如表(石灰石样品中含有的二氧化硅等杂质不溶于水也不与稀盐酸反应)
实验次数 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
1 | 10 | 7.5 |
2 | 10 | 5.0 |
3 | 10 | 3.2 |
4 | 10 | a |
根据实验数据计算:
(1)表中a的数值为;
(2)样品中碳酸钙的质量分数是;
(3)求盐酸中溶质的质量分数.
【答案】
(1)3.2
(2)68%
(3)
设20g稀盐酸中溶质的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73
2.5g x
![]()
x=1.825g
稀盐酸中溶质的质量分数为: ![]() ×100%=18.25%.
×100%=18.25%.
答:稀盐酸中溶质的质量分数为18.25%.
【解析】(1)根据表中数据可以知道,前两次减少的固体的质量均为5g,这说明10g稀盐酸和2.5g碳酸钙恰好完全反应,而第三次只减少1.8g,说明此时碳酸钙已反应完全,所以可以判断a的值为3.2;(2)石灰石样品中碳酸钙的质量分数是:![]() ×100%=68%.
×100%=68%.
【考点精析】利用根据化学反应方程式的计算对题目进行判断即可得到答案,需要熟知各物质间质量比=系数×相对分子质量之比.

【题目】在学习酸的化学性质后,同学们做了如图所示的A、B两个实验: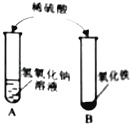
(1)A试管中发生反应的化学方程式 . 向B试管中的加入足量的稀硫酸,观察到的现象是 .
(2)实验结束后,小红将A、B两试管中的废液倒入同一洁净的烧杯中,片刻后发现烧杯中出现了红褐色沉淀,经分析,红褐色沉淀是氢氧化铁.
小红将烧杯中物质进行过滤得到无色滤液,滤液中含有什么溶质?小红、小军对此进行探究.
【实验讨论】
①小红分析了反应物和生成物之后,认为滤液中不可能有H2SO4 , 因为 .
②小军认为滤液中不可能有Fe2(SO4)3 , 理由是 .
(3)【提出猜想】
猜想Ⅰ:Na2SO4 NaOH
猜想Ⅱ:
(4)【设计实验】
实验操作 | 实验现象 | 结论 |
取少量滤液于试管中,向其中滴加酚酞试液 | 猜想Ⅰ成立 |

