题目内容
12.某校科学兴趣小组的同学在阅读资料时发现,18世纪末,法国科学家拉瓦锡曾经做了这样一个实验:让水蒸气通过一根烧红的铁管,生成了一种气体.同学们对这个实验很感兴趣.【提出问题】
红热的铁与水蒸气反应生成的气体是什么?
【作出猜想】
猜想1:生成的气体可能是氧气.
猜想2:生成的气体可能是氢气.
【实验探究】
为验证生成的气体是什么,该组同学在老师的指导下,设计了如图实验装置,并收集反应产生的气体(注:装置中必要的铁架台、铁夹、铁圈、石棉网、加热设备等在图中均已略去).A试管内装有铁粉,B烧瓶中装有一定量的水,提供反应所需水蒸气.

(1)该图中需加热的装置为A、B (填字母).
(2)图中C装置在实验中起到了安全瓶的作用.若没有C装置,实验结束时,先熄灭加热设备,再把导管移出水面,这样操作可能会导致水倒流入A装置,使试管炸裂.
(3)图中D装置收集气体的方法是排水集气法.
【结论】
(4)该组同学对所收集的气体进一步实验发现:该气体不溶于水,比空气轻,并且能燃烧.请你通过分析反应物的组成,结合实验现象,判断猜想2成立.
(5)该反应在生成气体的同时,还生成了一种黑色粉末状固体,则组成黑色固体的元素应该是Fe、O(填元素符号).
分析 可以根据实验目的判断物质的作用,根据物质的元素组成可以判断生成物的种类,根据物质的性质可以设计探究实验.
解答 解:(1)根据题目提供的信息(让水蒸气通过一根烧红的枪管)判定A装置中的铁粉必须加热,B装置也必须加热使水变成水蒸气因为是铁和水蒸气的反应.
(2)熄灭加热设备,会造成加热装置内温度降低,压强减小,若没有C装置会造成倒吸,水直接进入A装置.
(3)图中D装置收集气体的方法是排水集气法.
(4)根据质量守恒定律,反应物中只含Fe、O、H三种元素,生成的气体也就只有两种可能:H2或O2;根据气体的性质可确定是H2.
(5)因为此反应是铁和水发生的反应根据质量守恒定律反应前后元素种类不变,可确定生成的固体中一定含有Fe、O元素.
故答案是:(1)A、B;(2)水倒流入A装置,使试管炸裂;(3)排水集气法;(4)2;(5)Fe、O.
点评 解答本题要掌握实验的目的和实验的过程,只有这样才能对问题做出正确的判断.

练习册系列答案
 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
2.下列物质的鉴别方法选择不正确的是( )
| 待鉴别的物质 | 方法 | |
| A | 二氧化碳和空气 | 闻气味 |
| B | 水和双氧水 | 加入二氧化锰观察是否有气泡 |
| C | 鉴别高锰酸钾和碱式碳酸铜 | 观察颜色 |
| D | 蒸馏水和食盐水 | 取样,蒸发,观察是否有残留物 |
| A. | A | B. | B | C. | C | D. | D |
20.下列实验基本操作正确的是( )
| A. |  点燃酒精灯 | B. |  倾倒液体 | C. |  读取液体体积 | D. |  滴加液体 |
7.根据你的生活经验和所学的化学知识,判断下列做法正确的是( )
| A. | 用汽油清洗衣服上的油渍 | |
| B. | 深埋废弃塑料制品,可减少“白色污染” | |
| C. | 为节约成本,工业“三废”无需处理即可排放 | |
| D. | 用点燃的方法,除去二氧化碳中混有的少量一氧化碳 |
4.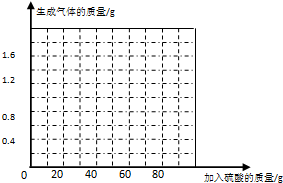 某化学兴趣小组的同学为测定假黄金(铜锌合金)组成元素的质量分数,取四份相同质量的样品分别放入等质量的烧杯中,然后分别加入稀硫酸,充分反应后用天平称量,几次试验数据如下:
某化学兴趣小组的同学为测定假黄金(铜锌合金)组成元素的质量分数,取四份相同质量的样品分别放入等质量的烧杯中,然后分别加入稀硫酸,充分反应后用天平称量,几次试验数据如下:
请回答下列问题并计算:(写出计算过程)
(1)经分析,在第1次实验结束后,反应物硫酸全反应完了.
(2)样品中锌的质量分数为多少?(请写出具体计算过程,注意格式)
(3)请在图中画出加入稀硫酸的质量与生成气体的质量的变化关系.
 某化学兴趣小组的同学为测定假黄金(铜锌合金)组成元素的质量分数,取四份相同质量的样品分别放入等质量的烧杯中,然后分别加入稀硫酸,充分反应后用天平称量,几次试验数据如下:
某化学兴趣小组的同学为测定假黄金(铜锌合金)组成元素的质量分数,取四份相同质量的样品分别放入等质量的烧杯中,然后分别加入稀硫酸,充分反应后用天平称量,几次试验数据如下:| 试验次序 | 第1次 | 第2次 | 第3次 | 第4次 |
| 所取样品的质量/g | 50.0 | 50.0 | 50.0 | 50.0 |
| 加入稀硫酸的质量/g | 20.0 | 40.0 | 60.0 | 80.0 |
| 生成气体的质量/g | 0.4 | 0.8 | 1.0 | 1.0 |
(1)经分析,在第1次实验结束后,反应物硫酸全反应完了.
(2)样品中锌的质量分数为多少?(请写出具体计算过程,注意格式)
(3)请在图中画出加入稀硫酸的质量与生成气体的质量的变化关系.





