题目内容
4. 某化学兴趣小组的同学为测定假黄金(铜锌合金)组成元素的质量分数,取四份相同质量的样品分别放入等质量的烧杯中,然后分别加入稀硫酸,充分反应后用天平称量,几次试验数据如下:
某化学兴趣小组的同学为测定假黄金(铜锌合金)组成元素的质量分数,取四份相同质量的样品分别放入等质量的烧杯中,然后分别加入稀硫酸,充分反应后用天平称量,几次试验数据如下:| 试验次序 | 第1次 | 第2次 | 第3次 | 第4次 |
| 所取样品的质量/g | 50.0 | 50.0 | 50.0 | 50.0 |
| 加入稀硫酸的质量/g | 20.0 | 40.0 | 60.0 | 80.0 |
| 生成气体的质量/g | 0.4 | 0.8 | 1.0 | 1.0 |
(1)经分析,在第1次实验结束后,反应物硫酸全反应完了.
(2)样品中锌的质量分数为多少?(请写出具体计算过程,注意格式)
(3)请在图中画出加入稀硫酸的质量与生成气体的质量的变化关系.
分析 锌和稀硫酸反应生成硫酸锌和氢气,由表中数据可知,锌和稀硫酸反应生成氢气的质量是1g,根据氢气的质量可以计算锌的质量,进一步可以计算样品中锌的质量分数.
解答 解:(1)由第一次和第二次反应的过程可知,在第1次实验结束后,反应物硫酸全反应完了.
故填:硫酸.
(2)设锌的质量为x,
Zn+H2SO4═ZnSO4+H2↑,
65 2
x 1.0g
$\frac{65}{x}$=$\frac{2}{1.0g}$,
x=32.5g,
样品中锌的质量分数为:$\frac{32.5g}{50g}$×100%=65%,
答:样品中锌的质量分数为65%.
(3)由图中数据可知,加入50g稀硫酸时恰好完全反应,加入稀硫酸的质量与生成气体的质量的变化关系溶液下图所示: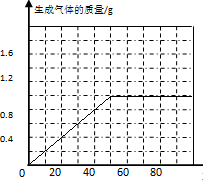
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析数据的能力,计算时要注意规范性和准确性.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
15.衡量物质在水中溶解性强弱的物理量为( )
| A. | 物质在水中的溶解度 | B. | 饱和溶液的溶质质量分数 | ||
| C. | 物质的相对分子质量 | D. | 物质水溶液的密度 |
19.为了防止空气污染,保护美丽的蓝色天空,洁净的空气对人类非常重要.下列做法不利于保护大气的是 ( )
| A. | 使用清洁能源代替煤和石油 | B. | 积极植树造林,防止扬尘污染 | ||
| C. | 焚烧落叶和垃圾 | D. | 工业废气处理后排放 |
2.我们每天早晨喝一杯豆浆,为人体内补充的营养素是( )
| A. | 蛋白质 | B. | 糖类 | C. | 油脂 | D. | 维生素 |
