题目内容
4.为测定某稀硫酸中溶质的质量分数,某同学将10gCu-Zn合金放入到盛有40g稀硫酸的烧杯中,恰好完全反应后,测得烧杯中剩余物的质量为49.9g.(1)Cu-Zn合金外表酷似黄金,又被称为“假黄金”,相对于其成分金属,具有的特点为硬度增大熔点降低.
(2)计算稀硫酸中溶质的质量分数.
分析 (1)根据合金的特性解答;
(2)根据铜不能和稀硫酸反应,锌和稀硫酸反应生成硫酸锌和氢气,反应前后的质量差即为反应生成氢气的质量,根据反应的化学方程式和提供的数据可以进行相关方面的计算.
解答 解:
(1)Cu-Zn合金外表酷似黄金,又被称为“假黄金”,相对于其成分金属,具有的特点为硬度增大熔点降低;
(2)生成氢气的质量为:10g+40g-49.9g=0.1g,
设硫酸的质量为x,
Zn+H2SO4═ZnSO4+H2↑,
98 2
x 0.1g
$\frac{98}{x}=\frac{2}{0.1g}$
x=4.9g,
该稀硫酸的溶质质量分数为:$\frac{4.9g}{40g}$×100%=12.25%,
答案:(1)硬度增大熔点降低; (2)12.25%.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出氢气的质量是正确解答本题的前提和关键.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
12.初中化学中几个有趣又富有科学价值的实验如下所示,下列结论错误的是( )
| 选项 | A | B | C | D |
| 实验 | 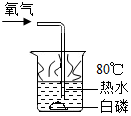 | 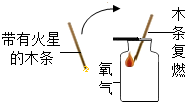 | 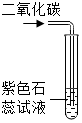 | 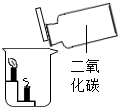 |
| 现象 | 热水中未燃烧的白磷在通入氧气后燃烧 | 带火星的木条伸入氧气中复燃 | 紫色石蕊试液在通入二氧化碳后变红 | 燃烧的蜡烛由低到高依次熄灭 |
| 结论 | 燃烧需要氧气 | 氧气浓度越大,燃烧越剧烈 | 使石蕊变红的是二氧化碳 | 二氧化碳密度比空气大,既不可燃也不助燃 |
| A. | A | B. | B | C. | C | D. | D |
19.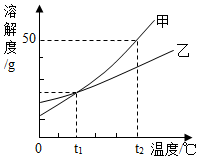 图为甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
图为甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
 图为甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
图为甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )| A. | 甲物质的溶解度大于乙物质的溶解度 | |
| B. | 甲中含有少量的乙,可以用蒸发溶剂的方法提纯乙 | |
| C. | t2℃时,将等质量的甲、乙两种物质的溶液分别降温至t1℃,析出晶体的质量甲一定大于乙 | |
| D. | t2℃时,乙饱和溶液中溶质的质量分数一定小于甲饱和溶液中溶质的质量分数 |
11.对比实验是化学学习中行之有效的思维方法.下列设计中能达到目的是(已知浓氨水显碱姓,能使无色酚酞试液变紅色)( )
| A. | 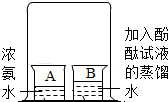 实验的设计是为了探究分子之间是有间隔的 | |
| B. | 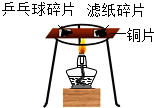 探究的是可燃物燃烧是否需要达到一定温度 | |
| C. | 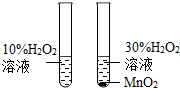 探究的是MnO2对H2O2分解的催化作用 | |
| D. |  探究的是可燃物燃烧是否需要与氧气充分接触 |