题目内容
1. 碳酸钙是常见的补钙剂,按照要求完成下列计算:
碳酸钙是常见的补钙剂,按照要求完成下列计算:(1)碳酸钙中钙元素的质量分数为40%.
(2)如图所示是某钙片的部分信息,同学要通过如下实验测定该钙片的钙元素含量是否符合标签标注:取10片钙片投入50g稀盐酸中(盐酸足量),反应停止后测得烧杯中物质总量为53.9g.
分析 (1)根据碳酸钙的化学式求算钙元素的质量分数;
(2)根据质量守恒定律可知,过程中质量的减少是因为生成了二氧化碳,所以可以求算二氧化碳的质量,根据二氧化碳的质量和对应的化学方程式求算碳酸钙的质量,进而求算每一片钙片对应的钙元素的质量,进而和标签对比.
解答 解:碳酸钙中钙元素的质量分数为$\frac{40}{40+12+16×3}$×100%=40%
根据质量守恒定律可得,生成的二氧化碳的质量为10×0.5g+50g-53.9g=1.1g
设碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 1.1g
$\frac{100}{44}$=$\frac{x}{1.1g}$
x=2.5g
则钙元素的质量为2.5g×40%=1g
每片含钙元素1g÷10=0.1g符合标签标注.
答:
(1)碳酸钙中钙元素的质量分数为40%;
(2)该钙片的钙元素含量符合符合标签标注.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
相关题目
9.经测定,在任何水溶液中,均存在一定数量的H+【用n(H+)表示】和一定数量的OH-【用n(OH-)表示】,n(H+)与n(OH-)的相对大小对应溶液的酸碱性如表所示:
据此分析
(1)常温下测得水中pH=7,可知水中n(H+)=n(OH-)(填“>”或“=”或“<”,下同).
(2)向盛有碳酸钠溶液的试管中滴入几滴酚酞,现象是溶液变为红色,原因是该溶液中n(H+)<n(OH-).
(3)往上述试管中再滴入适量的硫酸氢钠溶液,溶液颜色褪去,说明硫酸氢钠溶液中n(H+)>n(OH-).
(4)通过上述信息,由此得出盐溶液一定显中性是否正确?错误(填“正确”或“错误”).
| n(H+)与n(OH-)的相对大小 | 溶液的酸碱性 |
| n(H+)>n(OH-) | 酸性 |
| n(H+)=n(OH-) | 中性 |
| n(H+)<n(OH-) | 碱性 |
(1)常温下测得水中pH=7,可知水中n(H+)=n(OH-)(填“>”或“=”或“<”,下同).
(2)向盛有碳酸钠溶液的试管中滴入几滴酚酞,现象是溶液变为红色,原因是该溶液中n(H+)<n(OH-).
(3)往上述试管中再滴入适量的硫酸氢钠溶液,溶液颜色褪去,说明硫酸氢钠溶液中n(H+)>n(OH-).
(4)通过上述信息,由此得出盐溶液一定显中性是否正确?错误(填“正确”或“错误”).
9.归纳与比较”是化学学习的主要方法.下列关于CO2与CO的不同点比较错误的是( )
| A. | 组成:组成元素相同,碳元素的化合价不同 | |
| B. | 性质:CO2能溶于水,与水反应生成碳酸; CO难溶于水,但能燃烧 | |
| C. | 用途:CO2可用于光合作用、灭火等; CO可作气体燃料,还可用于人工降雨 | |
| D. | 危害:CO2会造成“温室效应”; CO易与血液中的血红蛋白结合引起中毒 |
6.亮亮做家务时接触到下列用品,请分析回答问题.
(1)清理垃圾时,亮亮发现一袋脱氧剂,拆开后看到还原铁粉已生锈,铁粉生锈的原因是Fe与潮湿的空气接触.
(2)亮亮刷洗马桶时,不小心将洁厕灵倒在大理石地砖上,可能看到的现象是产生气泡.
(3)亮亮清洗炉灶时戴上橡胶手套,以防清洁剂与皮肤直接接触,其原因是NaOH有强腐蚀性.
| 用品 | 脱氧剂 | 洁厕灵 | 炉灶清洁剂 |
| 有效成分 | 还原铁粉 | 盐酸 | 氢氧化钠 |
(2)亮亮刷洗马桶时,不小心将洁厕灵倒在大理石地砖上,可能看到的现象是产生气泡.
(3)亮亮清洗炉灶时戴上橡胶手套,以防清洁剂与皮肤直接接触,其原因是NaOH有强腐蚀性.
11.下列物质间的转化,能一步实现的是( )
| A. | Fe→FeCl3 | B. | CaCO3→Ca(OH)2 | C. | H2O2→H2 | D. | Cu(OH)2→CuCl2 |
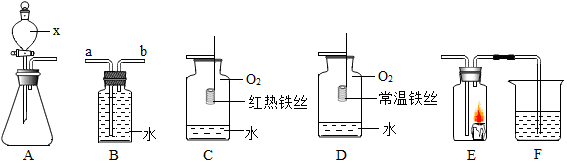

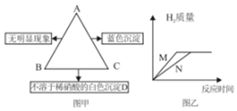 有A、B、C三种物质,已知A是一种氯化物(RCl2),B是一种酸,C是一种碱.图甲表示A、B、C三种物质的溶液两两混合时的实验现象,请回答:
有A、B、C三种物质,已知A是一种氯化物(RCl2),B是一种酸,C是一种碱.图甲表示A、B、C三种物质的溶液两两混合时的实验现象,请回答: