题目内容
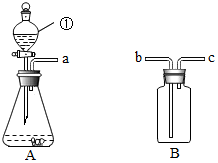
10.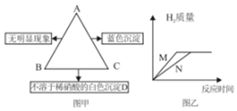 有A、B、C三种物质,已知A是一种氯化物(RCl2),B是一种酸,C是一种碱.图甲表示A、B、C三种物质的溶液两两混合时的实验现象,请回答:
有A、B、C三种物质,已知A是一种氯化物(RCl2),B是一种酸,C是一种碱.图甲表示A、B、C三种物质的溶液两两混合时的实验现象,请回答:(1)D的化学式为BaSO4;
(2)A、C反应的化学方程式为Ba(OH)2+CuCl2=BaCl2+Cu(OH)2↓;
(3)如图乙,若等质量的M、N分别为铁和锌中的一种,分别与等质量、等溶质质量分数的B溶液反应,产生氢气的质量与反应时间的关系如图乙所示,则M为锌,反应结束后只有一种金属有剩余,则剩余金属为铁.(相对原子质量:Fe-56 Zn-65)
分析 根据A,B,C三种物质,A是一种氯化物,B是一种酸,C是一种碱,A和C反应会生成蓝色沉淀,所以A是氯化铜,C和B反应会生成不溶于酸的白色沉淀,C是氢氧化钡,B是硫酸,然后将推出的物质进行验证即可.
解答 解:(1)A,B,C三种物质,A是一种氯化物,B是一种酸,C是一种碱,A和C反应会生成蓝色沉淀,C和B反应会生成不溶于酸的白色沉淀,所以A是氯化铜,C是氢氧化钡,B是硫酸,经过验证,推导正确,所以D是氢氧化钡和硫酸生成的硫酸钡沉淀,化学式为:BaSO4;
(2)A、C的反应是氯化铜和氢氧化钡反应生成氢氧化铜沉淀和氯化钡,化学方程式为:Ba(OH)2+CuCl2=BaCl2+Cu(OH)2↓;
(3)若M、N分别为铁和锌中的一种,分别与等质量、等溶质质量分数的稀硫酸溶液反应,则金属全部参加反应,产生氢气的质量一样,产生氢气的质量M快,所以M金属活泼,则M为锌,生成等质量的氢气需要的铁的质量小于锌的质量,每65份质量的锌会生成2份质量的氢气,每56份质量的铁会生成2份质量的氢气,所以反应结束后只有一种金属有剩余,则剩余金属为铁.
故答案为:
(1)BaSO4;(2)Ba(OH)2+CuCl2=BaCl2+Cu(OH)2↓;(3)锌,铁.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案
相关题目
5.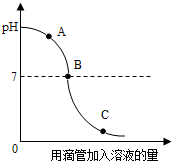 实验小组探究盐酸和氢氧化钠反应过程中溶液pH的变化规律,得到如图所示曲线,下列有关该实验事实的说法正确的是( )
实验小组探究盐酸和氢氧化钠反应过程中溶液pH的变化规律,得到如图所示曲线,下列有关该实验事实的说法正确的是( )
 实验小组探究盐酸和氢氧化钠反应过程中溶液pH的变化规律,得到如图所示曲线,下列有关该实验事实的说法正确的是( )
实验小组探究盐酸和氢氧化钠反应过程中溶液pH的变化规律,得到如图所示曲线,下列有关该实验事实的说法正确的是( )| A. | B点表示此时溶液为纯净物 | |
| B. | A点时的溶液能使酚酞试液变红 | |
| C. | C点时,溶液中溶质只有氯化氢 | |
| D. | 该实验是将氢氧化钠溶液滴入盐酸中 |
19.最近调查发现不少的中学生长期挑食、偏食不利于身体的健康,我们每天摄入的食物必须注意合理搭配.下列食物中富含维生素的是( )
| A. | 鸡肉 | B. | 草鱼 | C. | 大米 | D. | 白菜 |
 碳酸钙是常见的补钙剂,按照要求完成下列计算:
碳酸钙是常见的补钙剂,按照要求完成下列计算: