题目内容
4. 在加热条件下,炭粉可以还原某些金属氧化物,得到金属单质.小明同学设计了如图1所示的实验来研究氧化铜跟活性炭的反应,实验的装置和现象如下:
在加热条件下,炭粉可以还原某些金属氧化物,得到金属单质.小明同学设计了如图1所示的实验来研究氧化铜跟活性炭的反应,实验的装置和现象如下:实验中观察到:黑色粉末变红色,澄清石灰水变浑浊.
小明根据上述现象认为:碳还原氧化铜可以生成铜和二氧化碳.
【提出疑问】“碳燃烧时可能生成CO2也可能生成CO,那么碳与氧化铜反应生成的气体是否也有多种可能?”
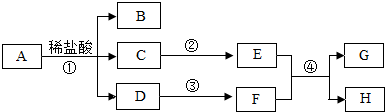
【设计实验】小雨同学打算用如图2的一些实验装置设计一套组合装置以检测碳还原氧化铜时生成的气体的成分.

若要证明碳还原氧化铜生成的气体中是否含有CO和CO2,上述装置的连接顺序是(装置可重复使用):A→B→D→F→C→B→D.
实验中根据什么现象可判断产生的气体中含CO?在实验中,若装置C中的黑色粉末变红色,则有一氧化碳气体产生
【反思】小明认为上述装置存在不完善之处,你认为装置还需如何改进?在装置D上装上一个气球,收集未反应的一氧化碳气体,防止污染空气.
分析 根据实验中所出现的“澄清石灰水变浑浊”,可判断反应后有二氧化碳气体放出;
【设计实验】要证明碳还原氧化铜生成的气体中是否含有CO和CO2,可把气体先通过氢氧化钠溶液除去二氧化碳,然后再通入灼热的氧化铜并再次使用澄清石灰水进行气体二氧化碳的检验,若观察到澄清石灰水变浑浊,可证明生成的气体中含有CO;
【反思】CO气体有毒,不经处理而把混有CO的气体直接排放会形成空气污染,因此,装置存在不足;
解答 解:碳还原氧化铜生成使澄清石灰水变浑浊的二氧化碳气体;
【设计实验】把还原氧化铜后的气体通过澄清石灰水检验气体中的二氧化碳后通过氢氧化钠溶液除去二氧化碳,为确定二氧化碳已完全除去可再次通过澄清石灰水进行验证;确定气体中不含二氧化碳后使用浓硫酸对气体进行干燥,干燥后的气体能过灼热的氧化铜,如果气体中含有CO则黑色氧化铜变成红色,把反应后气体再通入澄清石灰水,石灰水应变浑浊;通过以上过程可证明气体为一氧化碳和二氧化碳的混合气体;
故答案为:A→B→D→F→C→B→D;
气体通入灼热氧化铜前的装置B(即第二个B)中澄清石灰水不浑浊说明气体中的二氧化碳已全部除去;通过灼热氧化铜后盛放澄清石灰水(即第三个B)变浑浊可说明生成了二氧化碳,同时可观察C中黑色固体变红色;据此可说明气体中含有CO;
【反思】反应后产生的尾气中含有有毒气体CO,直接排放会造成空气污染,因此需要对尾气进行收集或直接燃烧处理;而装置中缺少类似的处理装置;
故答案为:在装置最后放一盏酒精灯,点燃尾气;
答案:
二氧化碳
【设计实验】B D C B D; 在实验中,若装置C中的黑色粉末变红色,则有一氧化碳气体产生
【反思】在装置D上装上一个气球,收集未反应的一氧化碳气体,防止污染空气.
点评 在研究物质组成时,通过定性的探究实验不能确定某组成成分时,可通过定量研究加以判断;定量研究时,质量守恒思想是进行推断的根本依据.

| 项目 | 物质 | 杂质(少量) | 试剂 | 操作方法 |
| A | KCl | MnO2 | 足量的水 | 溶解、过滤、蒸发 |
| B | CO2 | 水蒸气 | 足量的NaOH固体 | 洗气 |
| C | FeSO4溶液 | CuSO4溶液 | 适量的NaOH溶液 | 过滤 |
| D | CO | CO2 | 足量氧化铜粉末 | 加热 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 实验室用过氧化氢溶液制氧气 H2O2$\stackrel{MnO_{2}}{→}$ H2+O2 分解反应 | |
| B. | 拉瓦锡测定空气中氧气的含量 P+O2 $\stackrel{点燃}{→}$ P2O5 化合反应 | |
| C. | 冬季燃煤产生有刺激性气味的气体 S+O2$\stackrel{点燃}{→}$SO2 化合反应 | |
| D. | 实验室用氯酸钾制氧气 KClO3$\stackrel{△}{→}$KCl+O2 分解反应 |
| A. | 溶液质量都减少,溶质的质量分数都减小 | |
| B. | 溶液质量都增大,溶质的质量分数都减小 | |
| C. | 溶液质量一个增大,一个减小;溶质的质量分数一个增大,一个减小 | |
| D. | 溶液质量一个增大,一个减小;溶质的质量分数都减小 |
| A. | 混合气体中肯定没有氢气、水蒸气 | B. | 混合气体中一定有氯化氢 | ||
| C. | 混合气体中可能有二氧化碳 | D. | 混合气体中可能有一氧化碳 |