题目内容
10.纳米碳酸钙常用做牙膏摩擦剂,如图是某厂生产纳米碳酸钙的工艺流程.(1)碳酸钙中碳元素的化合价为+4价.
(2)将氯化钙制成溶液,目的是增大反应物接触面积,加快反应速度.
(3)该工艺中需要大量二氧化碳,工业上通常用高温煅烧石灰石的方法获得,写出反应化学方程式CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,其中另一种生成物俗称生石灰,请指出它的一种用途做干燥剂.
(4)上述过程制得的纳米碳酸钙粗品表面可能含有的可溶性杂质有NH4Cl(或CaCl2)(写一种化学式即可)

分析 (1)根据在化合物中正负化合价代数和为零进行计算;(2)将氯化钙制成溶液可以增大反应物接触面积,加快反应速度;(3)碳酸钙高温生成氧化钙和二氧化碳,氧化钙俗称生石灰,常用来做干燥剂;(4)由于碳酸钙粗品是从氯化钙溶液中过滤出来的,所以表面可能含有的可溶性杂质是氯化铵,如果氯化钙溶液过量的话,表面可能含有氯化钙.
解答 解:(1)设碳元素的化合价是x则:+2+x+(-2)×3=0解得x=+4;
(2)将氯化钙制成溶液可以增大反应物接触面积,加快反应速度;
(3)碳酸钙高温生成氧化钙和二氧化碳,反应条件是高温,所以方程式是:CaCO3高温?CaO+CO2↑;氧化钙俗称生石灰,常用来做干燥剂;
(4)由于碳酸钙粗品是从氯化钙溶液中过滤出来的,所以表面可能含有的可溶性杂质是氯化铵,如果氯化钙溶液过量的话,表面可能含有氯化钙;
故答案为:(1)+4;(2)增大反应物接触面积,加快反应速度;(3)CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;生石灰;做干燥剂;NH4Cl(或CaCl2).
点评 解答本题关键是要知道反应物的接触面积越大,反应速度越快,知道化学方程式的书写方法:一写、二配、三注明、四等号.

练习册系列答案
相关题目
20.下列做法错误的是( )
| A. | 用汽油溶解油脂的方法除去衣服上的油污 | |
| B. | 用适量的熟石灰改良酸性土壤 | |
| C. | 用喷漆的方法防止自行车支架锈蚀 | |
| D. | 用食盐配制生理盐水 |
18.下列常见食物中,富含糖类的是( )
| A. | 鸡蛋 | B. | 黄瓜 | C. | 豆油 | D. | 米饭 |
5.百合具有润肺止咳,养颜美容等功效,百合中含有秋水仙碱,其化学式为C22H25NO6,下列说法正确的是( )
| A. | 秋水仙碱分子中碳、氢、氮、氧的原子个数比为22:25:1:6 | |
| B. | 秋水仙碱中氢元素的质量分数最大 | |
| C. | 秋水仙碱完全燃烧只生成二氧化碳和水 | |
| D. | 一个秋水仙碱分子由22个碳原子、25个氢原子、1个氮原子和3个氧分子构成 |
15.第四套人民币硬币中涉及到Fe、Cu、Ni(镍)等金属.已知:Ni+H2SO4═H2↑+NiSO4、Fe+NiCl2═Ni+FeCl2.下列关于三种金属的活动性由强到弱的顺序正确的是( )
| A. | Fe、Cu、Ni | B. | Ni、Fe、Cu | C. | Fe、Ni、Cu | D. | Cu、Ni、Fe |
 已知A-F都是初中化学中的常见物质,其中A和C是无色无味气体,B是黑色粉末,D是红色固体,它们的转化关系如图所示(部分生成物已省略)
已知A-F都是初中化学中的常见物质,其中A和C是无色无味气体,B是黑色粉末,D是红色固体,它们的转化关系如图所示(部分生成物已省略)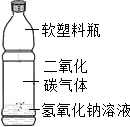 化学课堂上,同学们正在探究二氧化碳气体与碱溶液能否发生化学反应.
化学课堂上,同学们正在探究二氧化碳气体与碱溶液能否发生化学反应.