题目内容
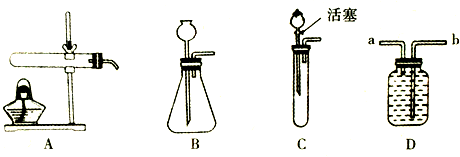
 如图是某同学设计的趣味实验装置,其气密性良好.
如图是某同学设计的趣味实验装置,其气密性良好.(1)若分液漏斗中的物质是稀盐酸,锥形瓶底放有石灰石,则旋转分液漏斗的活塞,滴入溶液后关闭活塞,能明显观察到哪些现象(写一条即可)?并写出有关反应的化学方程式.
(2)若分液漏斗中的物质是氢氧化钠溶液,锥形瓶内盛有二氧化碳气体,则旋转分液漏斗的活塞,滴入溶液后,可能会观察到什么现象?
考点:反应现象和本质的联系,酸的化学性质,碱的化学性质,书写化学方程式、文字表达式、电离方程式
专题:实验性简答题
分析:可以根据物质之间相互作用的情况判断实验现象,可以根据质量守恒定律正确的书写化学方程式.
解答:解:(1)稀盐酸与石灰石反应生成二氧化碳,会看到溶液中有气泡冒出,锥形瓶中气体增多,压强变大,U形管中红墨水右侧升高左侧降低;方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)因为氢氧化钠溶液能吸收二氧化碳气体从而使锥形瓶中的压强迅速减小,U形管中红墨水的液面左高右低(或被吸入锥形瓶中)等.
故答案为:(1)溶液中有气泡冒出(或U形管中红墨水右侧升高左侧降低);CaCO3+2HCl=CaCl2+H2O+CO2↑;(2)U形管中红墨水的液面左高右低.
(2)因为氢氧化钠溶液能吸收二氧化碳气体从而使锥形瓶中的压强迅速减小,U形管中红墨水的液面左高右低(或被吸入锥形瓶中)等.
故答案为:(1)溶液中有气泡冒出(或U形管中红墨水右侧升高左侧降低);CaCO3+2HCl=CaCl2+H2O+CO2↑;(2)U形管中红墨水的液面左高右低.
点评:解答本题的关键是要充分理解物质的性质和反应时的实验现象,只有这样才能对问题做出正确的判断.

练习册系列答案
相关题目
把含有CO、CO2、N2、H2的混合气体依次通过澄清石灰水、加热的氧化铜,冷却,若每次反应都是充分的,则最后得到的气体是( )
| A、N2 |
| B、N2和CO |
| C、N2和CO2 |
| D、H2 |
 2011年9月29日晚21时16分许,“长征二号F”T1型运载火箭托举着“天宫一号”直刺苍穹,把一团桔红色的烈焰留在了秋日的大漠长空.为实施空间交会对接试验提供目标飞行器.运送“天宫一号”的“长征二号F”T1运载火箭,火箭主要燃料是偏二甲肼(化学式为C2H8N2).下列有关偏二甲肼组成的叙述,正确的是( )
2011年9月29日晚21时16分许,“长征二号F”T1型运载火箭托举着“天宫一号”直刺苍穹,把一团桔红色的烈焰留在了秋日的大漠长空.为实施空间交会对接试验提供目标飞行器.运送“天宫一号”的“长征二号F”T1运载火箭,火箭主要燃料是偏二甲肼(化学式为C2H8N2).下列有关偏二甲肼组成的叙述,正确的是( )| A、由2个碳原子、4个氢气分子、一个氮气分子组成 |
| B、由碳、氢、氮三种元素组成 |
| C、由2个碳原子、8个氢原子、2个氮原子构成 |
| D、组成元素碳、氢、氮的质量比为1:4:1 |
某矿泉水标签上印有主要成分有:K(1.0~27.0)mg/L;Cl(1.0~24.0)mg/L.这里的K、Cl是指( )
| A、单质 | B、元素 |
| C、金属离子 | D、分子 |
下列关于空气成分的说法正确的是( )
| A、氧气约占空气质量的21% |
| B、饼干在空气中变软是因为空气中含有水蒸气 |
| C、稀有气体通电发光是化学变化 |
| D、空气中的氧气主要来自植物的呼吸作用 |