题目内容
14.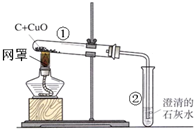 用木炭还原氧化铜的实验如图.
用木炭还原氧化铜的实验如图.(1)酒精灯加灯罩的目的聚拢火焰,使温度更高;
(2)加热一段时间后,可观察到的现象黑色粉末逐渐变成红色,澄清的石灰水变浑浊
(3)请你写出①②试管中发生反应的化学方程式:①C+2CuO $\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑、②CO2+Ca(OH)2=CaCO3↓+H2O.
分析 (1)木炭还原氧化铜实验需要高温,所以酒精灯上加网罩,可以聚拢火焰,提高温度;
(2)木炭能和氧化铜在高温条件下反应生成铜和二氧化碳,据此分析实验现象;
(3)据木炭和氧化铜反应原理及二氧化碳能和氢氧化钙反应生成碳酸钙和水书写方程式.
解答 解:(1)因为这个实验对温度的要求较高,所以加灯罩是为了聚拢火焰,使温度更高;
(2)木炭能和氧化铜在高温条件下反应生成铜和二氧化碳,发生的现象是黑色粉末逐渐变成红色,澄清的石灰水变浑浊;
(3)木炭能和氧化铜在高温条件下反应生成铜和二氧化碳,二氧化碳能和氢氧化钙反应生成碳酸钙和水,反应的化学方程式分别为:C+2CuO $\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑CO2+Ca(OH)2=CaCO3↓+H2O;
故答案为:(1)聚拢火焰,提高温度;
(2)黑色粉末逐渐变成红色;澄清的石灰水变浑浊;
(3)C+2CuO $\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑;CO2+Ca(OH)2=CaCO3↓+H2O.
点评 本题主要考查木炭的化学性质和化学方程式的书写等方面的知识,书写化学方程式时要注意遵循质量守恒定律.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
9.下列有关物质用途的表述错误的是( )
| A. | 铜可用作导线 | |
| B. | 葡萄糖可用于提供能量 | |
| C. | 明矾能够消毒杀菌是利用了明矾很强的氧化性 | |
| D. | 活性炭可以用于自来水的净化 |
5.下列关于二氧化碳的性质叙述中,正确的是( )
| A. | 能溶于水,水溶液显酸性 | |
| B. | 易溶于水,密度比空气大 | |
| C. | 能溶于水,有毒,能使人窒息而死 | |
| D. | 在某些反应中可作氧化剂,具有氧化性 |
2.下面四个图象分别对应四种操作过程,其中不正确的是( )
| A. |  向饱和KNO3溶液中加入KNO3 | |
| B. | 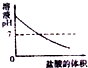 向NaOH溶液中滴加盐酸至过量 | |
| C. |  向CuCl2和HCl的混合溶液中加入加量NaOH溶液 | |
| D. |  向两份同体积和同质量分数的HCl溶液中分别加入足量的铁粉和镁粉 |
9.三种物质间只通过一步反应就能实现如箭头所指方向的转化,下列符合要求的组合是( )
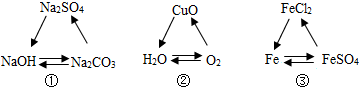

| A. | ①② | B. | ①③ | C. | ②③ | D. | ①②③ |
3.下列图象与对应选项关系不合理的是( )
| A. | 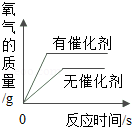 用等质量、等浓度的H2O2溶液在有、无催化剂条件下制取氧气 | |
| B. | 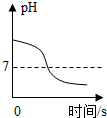 向一定量的NaOH溶液中不断地滴加稀盐酸 | |
| C. | 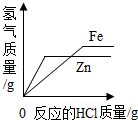 将等质量的镁粉、铁粉分别入到足量且溶质质量分数相同的稀硫酸中 | |
| D. | 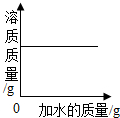 在某温度下,向一定量的食盐水中不断加水 |