题目内容
12.下列关于原子、分子的说法错误的是( )| A. | 分子可以构成物质,而原子只能构成分子 | |
| B. | 在化学变化中,分子可以分成原子,而原子不能再分 | |
| C. | 原子的质量主要集中在原子核上 | |
| D. | 由分子构成的物质,分子是保持物质化学性质的最小粒子 |
分析 抓住分子、原子的本质区别和联系及原子的结构.
解答 解:A、构成物质的微粒有:分子、原子和离子,故A说法错误;
B、在化学变化中,分子可以分成原子,而原子不能再分,故B说法正确;
C、原子的质量主要集中在原子核上,故C说法正确;
D、由分子构成的物质,分子是保持物质化学性质的最小粒子,故D说法正确.
故选A.
点评 主要考查了分子、原子的本质区别和联系及有关原子的结构,培养学生的微粒观.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
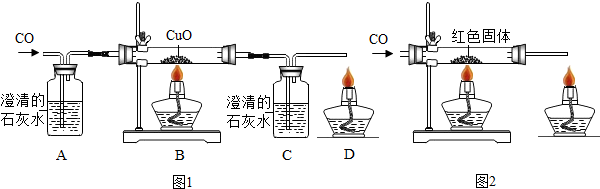
17.实验室用碱式碳酸铜[化学式:Cu2(OH)2CO3]制备氧化铜并检验其产物,装置如下:

步骤一:连接A和B,打开活塞,通入空气.
步骤二:关闭活塞,连上C和D,开始加热.
步骤三:在加热过程中,记录B中固体质量变化如下表,在t3时停止加热.
(1)步骤一通入空气的目的是排出硬质玻璃管B中的水蒸气和二氧化碳,防止干扰实验结果.
(2)C中试剂是无水硫酸铜(填名称);A的作用是吸收空气中的水蒸气和二氧化碳(填名称).
(3)选择t3时停止加热的理由是t3时与t2时相比,固体质量不再改变,说明碱式碳酸铜已完全分解.
(4)B中发生反应的化学方程式为:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+H2O+CO2↑.

步骤一:连接A和B,打开活塞,通入空气.
步骤二:关闭活塞,连上C和D,开始加热.
步骤三:在加热过程中,记录B中固体质量变化如下表,在t3时停止加热.
| 加热时间(min) | 0 | t1 | t2 | t3 |
| B中固体质量(g) | 6.66 | 5.20 | 4.80 | 4.80 |
(2)C中试剂是无水硫酸铜(填名称);A的作用是吸收空气中的水蒸气和二氧化碳(填名称).
(3)选择t3时停止加热的理由是t3时与t2时相比,固体质量不再改变,说明碱式碳酸铜已完全分解.
(4)B中发生反应的化学方程式为:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+H2O+CO2↑.
15.下列物质中属于酸式盐的是( )
| A. | K2CO3 | B. | NH4Cl | C. | NaHSO4 | D. | BaSO4 |
17.在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化如表.下列说法中正确的是.
A.该反应为化合反应 B.甲、乙两种物质间参加反应的质量比为1:4
C.丙可能为该反应的催化剂 D.乙、丁两种物质间反应的质量比为7:5.
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前物质质量/g | 8 | 32 | 5 | 4 |
| 反应后物质质量/g | 16 | 4 | x | 24 |
C.丙可能为该反应的催化剂 D.乙、丁两种物质间反应的质量比为7:5.
4.下列有关叙述中,正确的是( )
| A. | 可用肥皂水区别硬水和软水 | |
| B. | 要保护水资源,只能禁止使用化肥和农药 | |
| C. | 为了控制空气中PM2.5的含量应停止建筑工地施工 | |
| D. | 因为有了温室效应,全球平均地表温度才提高到适合人类生存的15℃ |
2.空气是人类活动必需的自然资源.工业上常用分离空气的方法制取氧气,如图1所示,实验室常用物质分解的方法制取氧气.

(1)写出标有序号的仪器名称:a分液漏斗,b集气瓶.
(2)在实验室中用过氧化氢溶液和二氧化锰混合制取并收集氧气,可选择BC或BE装置(填字母代号).
(3)学习了MnO2对过氧化氢分解有催化作用的知识后.某同学想:CuO能否起到类似MnO2的催化剂作用呢?于是进行了如下探究.
【猜想】Ⅰ.CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ.CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ.CuO是反应的催化剂,反应前后质量和化学性质都不变.
【实验】用天平称量0.2g CuO,取5mL 5%过氧化氢溶液于试管中,进行如图2实验:

(一)填表:
(二)步骤①的目的是与②进行对比;
(三)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、玻璃棒;
(四)过氧化氢能被CuO催化分解放出O2的化学方程式为2H2O2$\frac{\underline{\;氧化铜\;}}{\;}$2H2O+O2↑.
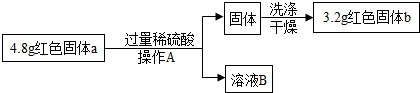
【拓展】要探究步骤⑤做过催化剂的CuO其它化学性质,还应补做的实验是用氢气(或一氧化碳或炭)还原固体,观察固体是否变成红色;或用加热的稀硫酸溶液固体,观察是否能生成蓝色溶液.

(1)写出标有序号的仪器名称:a分液漏斗,b集气瓶.
(2)在实验室中用过氧化氢溶液和二氧化锰混合制取并收集氧气,可选择BC或BE装置(填字母代号).
(3)学习了MnO2对过氧化氢分解有催化作用的知识后.某同学想:CuO能否起到类似MnO2的催化剂作用呢?于是进行了如下探究.
【猜想】Ⅰ.CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ.CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ.CuO是反应的催化剂,反应前后质量和化学性质都不变.
【实验】用天平称量0.2g CuO,取5mL 5%过氧化氢溶液于试管中,进行如图2实验:

(一)填表:
| 步骤③现象 | 步骤⑥结果 | 结论 |
| 带火星的木条复燃 | 固体质量是0.2g | 猜想Ⅰ、Ⅱ不成立 猜想Ⅲ成立 |
(三)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、玻璃棒;
(四)过氧化氢能被CuO催化分解放出O2的化学方程式为2H2O2$\frac{\underline{\;氧化铜\;}}{\;}$2H2O+O2↑.
【拓展】要探究步骤⑤做过催化剂的CuO其它化学性质,还应补做的实验是用氢气(或一氧化碳或炭)还原固体,观察固体是否变成红色;或用加热的稀硫酸溶液固体,观察是否能生成蓝色溶液.