题目内容
8.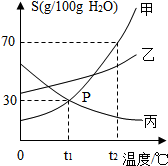 如图是甲、乙、丙三种物质(其晶体均不含结晶水)的溶解度曲线.据图回答:
如图是甲、乙、丙三种物质(其晶体均不含结晶水)的溶解度曲线.据图回答:(1)t1℃时甲、乙、丙三种物质的溶解度的大小关系是乙>甲=丙(或乙>丙=甲、甲=丙<乙、丙=甲<乙);
(2)甲中含有少量的乙时,可通过冷却(降温)结晶(或冷却热饱和溶液)的方法提纯甲.
(3)将t2℃时甲、乙、丙三种物质的饱和溶液各100g,均降温到t1℃.则三种溶液中溶剂的质量大小关系正确的是D(填选项).
A.乙>甲=丙 B.甲=乙>丙 C.甲>乙>丙 D.丙>乙>甲.
分析 根据物质的溶解度曲线,分析确定:
(1)t1℃时,三种物质的溶解度关系,比较物质的溶解度大小;
(2)由甲、乙的溶解度随温度变化而变化的情况,进而确定结晶析出的方法;
(3)降低温度时溶剂的质量不变,所以可由甲、乙、丙的溶解度在t2℃时的溶解度判断相同溶液中溶剂的质量大小关系分析解答.
解答 解:(1)t1℃时,三种物质的溶解度关系为乙>甲=丙;
(2)甲的溶解度受温度影响较大,乙的溶解度随温度变化较小,所以甲中含有少量的乙时,可通过冷却热饱和溶液或降温结晶的方法提纯甲;
(3)降低温度时溶剂的质量不变,所以可由甲、乙、丙的溶解度在t2℃时的溶解度判断相同溶液中溶剂的质量大小关系;t2℃时三种物质的溶解度由大到小的顺序是:甲>乙>丙,故相等的饱和溶液中溶剂质量关系是:丙>乙>甲.
故答案为:(1)乙>甲=丙;
(2)冷却热饱和溶液;
(3)D.
答案:
(1)乙>甲=丙 (或乙>丙=甲、甲=丙<乙、丙=甲<乙 )
(2)冷却(降温)结晶(或冷却热饱和溶液);
(3)D
点评 本题难度不大,主要考查了固体溶解度曲线所表示的意义,通过本题可以加强学生对固体溶解度的理解和应用、溶解度曲线的应用的理解,培养学生应用知识解决问题的能力.

练习册系列答案
 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案
相关题目
13.对下列化学用语中数字“2”的含义描述准确的是( )
| A. | 2O-“2”表示两个氧分子 | |
| B. | H2SO4-“2”表示一个硫酸分子中有两个氢元素 | |
| C. | Mg2+-“2”表示镁元素的化合价为+2价 | |
| D. | 2NO-“2”表示表示两个一氧化氮分子 |
20.化学实验中常常出现“1+l=2”或“l+l≠2”的有趣现象.下列符合“l+l=2”的事实是( )
| A. | 常温下,1L水与1L酒精混合后的体积等于2L | |
| B. | 室温下,1g镁与1g稀硫酸充分反应后所得的溶液质量为2g | |
| C. | 室温下,1g硫粉在lg氧气中完全燃烧后生成2g二氧化硫 | |
| D. | 20℃,lg氯化钠饱和溶液中加入1g氯化钠固体能得到2g氯化钠溶液 |
18.下列事实的结论或解释错误的是( )
| A. | 酸碱中和反应都能生成水--实质是H +与OH-结合生成H2O | |
| B. | 分离液态空气制氧气--说明分子可以再分 | |
| C. | 气体可压缩储存于钢瓶中--说明分子之间有间隔 | |
| D. | 桂花开放时满园飘香--说明分子在不断运动 |
18. 实验室常用双氧水与二氧化锰混合来制取氧气,写出相关反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,小王同学对“双氧水分解快慢的影响因素”进行了探究.
实验室常用双氧水与二氧化锰混合来制取氧气,写出相关反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,小王同学对“双氧水分解快慢的影响因素”进行了探究.
【提出问题】双氧水分解快慢的影响因素有哪些?
【猜想与假设】猜想一:可能与二氧化锰的形状有关;猜想二:可能与温度有关.
【设计并实验】小王同学用8mL3%的双氧水和二氧化锰进行了如下实验(反应进行10s时,H2O2均有剩余);
(1)欲探究温度对”双氧水分解快慢“是否有影响,应该比较a(或b)和c(或d)(填“a”“b”“c”或“d”)的大小;若粉末状二氧化锰催化效果好,那么b(或d)>c(或a)(填“a”“b”“c”或“d”)
(2)其他条件相同,双氧水浓度可能会影响催化效果,请你设计实验方案进行验证:相同温度下,取等体积浓度不同的双氧水分别于试管中,再分别加入等量形状相同的二氧化锰,比较10s内数据的氧气体积.
注意;若答对下列小题奖励4分,化学试卷总分不超过60分.
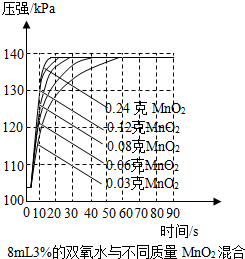
(3)小王同学还是用了压强传感器测不同质量二氧化锰对双氧水分解快慢的影响.他在8mL3%的双氧水中分别加入了0.03g,0.06g,0.08g,0.12g,0.24gMnO2.测得容器内压强的变化曲线如图所示(曲线的斜率表征催化反应的速率).请你观察图,并写出两条规律性结论:
①一定范围内,二氧化锰用量越多,双氧水分解越快;
②一定范围内,质量不同的二氧化锰在双氧水浓度、量相同的情况下,对最终产生氧气的量没有影响.
 实验室常用双氧水与二氧化锰混合来制取氧气,写出相关反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,小王同学对“双氧水分解快慢的影响因素”进行了探究.
实验室常用双氧水与二氧化锰混合来制取氧气,写出相关反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,小王同学对“双氧水分解快慢的影响因素”进行了探究.【提出问题】双氧水分解快慢的影响因素有哪些?
【猜想与假设】猜想一:可能与二氧化锰的形状有关;猜想二:可能与温度有关.
【设计并实验】小王同学用8mL3%的双氧水和二氧化锰进行了如下实验(反应进行10s时,H2O2均有剩余);
| 实验编号 | 温度℃ | 二氧化锰的形状(均取0.4cm) | 收集到氧气的体积/mL(时间均为10s) |
| ① | 20 | 颗粒状 | a |
| ② | 30 | 粉末状 | b |
| ③ | 30 | 颗粒状 | c |
| ④ | 20 | 粉末状 | d |
(2)其他条件相同,双氧水浓度可能会影响催化效果,请你设计实验方案进行验证:相同温度下,取等体积浓度不同的双氧水分别于试管中,再分别加入等量形状相同的二氧化锰,比较10s内数据的氧气体积.
注意;若答对下列小题奖励4分,化学试卷总分不超过60分.
(3)小王同学还是用了压强传感器测不同质量二氧化锰对双氧水分解快慢的影响.他在8mL3%的双氧水中分别加入了0.03g,0.06g,0.08g,0.12g,0.24gMnO2.测得容器内压强的变化曲线如图所示(曲线的斜率表征催化反应的速率).请你观察图,并写出两条规律性结论:
①一定范围内,二氧化锰用量越多,双氧水分解越快;
②一定范围内,质量不同的二氧化锰在双氧水浓度、量相同的情况下,对最终产生氧气的量没有影响.
19.下列有关实验现象的描述与事实不相符的是( )
| A. | 木炭在氧气中燃烧发出白光 | |
| B. | 硫在空气中燃烧发出明亮的蓝紫色火焰 | |
| C. | 铁丝在氧气中燃烧,火星四射,有黑色固体生成 | |
| D. | 蜡烛在空气中燃烧发出黄色火焰,稍有黑烟 |
3.下列实验不能达到实验目的是( )
| A. |  蒸发滤液 | B. |  探究生锈的探究 | ||
| C. |  称量氯化钠的质量 | D. |  证明二氧化碳与水反应生成碳酸 |