题目内容
16.化学用语是学习化学的重要工具.用化学用语表示:干冰CO2;碳酸根离子CO32-.分析 干冰是固态的二氧化碳,写出其化学式即可.
离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.
解答 解:干冰是固态的二氧化碳,其化学式为:CO2.
由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.碳酸根离子可表示为:CO32-.
故答案为:CO2;CO32-.
点评 本题难度不大,掌握常见化学用语(化学式、离子符号等)的书写方法是正确解答此类题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.甲、乙两科学研究小组安装两套如图1相同装置,来探究影响H2O2分解速率的因素.甲小组设计了如下实验方案,并得到如图2的实验数据,乙小组也设计了自己的实验方案来研究酸、碱对H2O2分解速率影响得到如图2的实验数据;
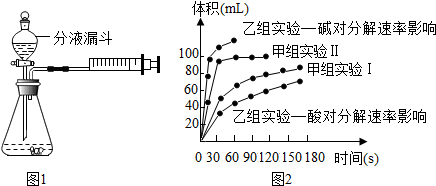
根据上述实验,请分析回答下列问题:
(1)根据甲小组的实验方案,甲小组是为了研究浓度对H2O2分解速率的影响;
(2)本实验是通过保持温度、催化剂不变,改变过氧化氢溶液的浓度来比较H2O2分解速率;
(3)根据实验数据分析,乙小组提出用BaO2固体与硫酸溶液反应制备H2O2,化学方程式:BaO2+H2SO4═BaSO4↓+H2O2,支持这一方案的理由是过氧化氢在酸性环境下分解较慢.
| 实验编号 | 温度 | 催化剂 | 质量分数 | |
| 甲组实验Ⅰ | 25℃ | 二氧化锰 | 10mL 2%H2O2 | |
| 甲组实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5%H2O2 |

根据上述实验,请分析回答下列问题:
(1)根据甲小组的实验方案,甲小组是为了研究浓度对H2O2分解速率的影响;
(2)本实验是通过保持温度、催化剂不变,改变过氧化氢溶液的浓度来比较H2O2分解速率;
(3)根据实验数据分析,乙小组提出用BaO2固体与硫酸溶液反应制备H2O2,化学方程式:BaO2+H2SO4═BaSO4↓+H2O2,支持这一方案的理由是过氧化氢在酸性环境下分解较慢.
7.玲玲在学习复分解反应时,对复分解反应的条件产生了兴趣,于是她和小组内的同学仅用以下药品展开了探究活动.
实验药品:稀硫酸、稀盐酸、氢氧化钠溶液、碳酸钠溶液、硝酸钡溶液、
氯化钠溶液、酚酞溶液
【提出问题】复分解反应发生的条件是什么?
【查阅资料】硝酸钡溶液显中性,且Ba2+有毒.
【实验探究】玲玲用上述物质做了下列几组实验.
【记录和解释】(1)组合①、②、⑤均无明显现象,其中组合①与另外两组的实质不同.为证明该不同之处,玲玲在实验过程中使用了酚酞溶液.
(2)请写出组合④的化学方程式H2SO4+Ba(NO3)2=BaSO4↓+2HNO3.
【实验结论】他们请教老师并讨论后知道,只有当两种化合物互相交换成分,生成物中有沉淀或水或气体生成时,复分解反应才可以发生.
【应用】写出利用熟石灰鉴别化肥氯化铵和氯化钾有关反应的化学方程式2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.
【拓展延伸】实验结束后,他们将所有废液收集在废液缸中静置,观察到白色沉淀和无色的上层清液.为了确定沉淀和清液的成分,继续展开探究.
【实验1】探究沉淀的成分.
【提出猜想】Ⅰ.沉淀只有硫酸钡Ⅱ.沉淀只有碳酸钡Ⅲ.沉淀中含有硫酸钡和碳酸钡.梅梅取少量沉淀于试管中,滴加过量的稀盐酸,观察到的现象是沉淀部分溶解,有气泡产生,证明了猜想Ⅲ是正确的.
【实验2】探究清液的成分.
①取少量清液于试管中,向其中滴加几滴硝酸钡溶液,无明显现象.
②另取少量清液于另一只试管中,滴加几滴稀硫酸,有白色沉淀产生.
【解释与结论】探究活动结束后,小组内成员通过讨论分析,一致认为清液中含有的离子除Na+、Cl-外,还有NO3-、Ba2+(指示剂除外).
【处理废液】为了防止污染环境,玲玲向废液缸中加入适量的碳酸钠溶液,对废液进行处理后,将固体回收进一步处理,溶液排放.
【交流与反思】根据你对物质溶解性的了解,结合复分解反应发生的条件,请写出一种在水溶液中一般不能发生复分解反应的可溶性盐NaNO3(写化学式).
实验药品:稀硫酸、稀盐酸、氢氧化钠溶液、碳酸钠溶液、硝酸钡溶液、
氯化钠溶液、酚酞溶液
【提出问题】复分解反应发生的条件是什么?
【查阅资料】硝酸钡溶液显中性,且Ba2+有毒.
【实验探究】玲玲用上述物质做了下列几组实验.
| 组合序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 组合物质 | H2SO4 NaOH | H2SO4 NaCl | H2SO4 Na2CO3 | H2SO4 Ba(NO3)2 | NaOH Ba(NO3)2 | Na2CO3 Ba(NO3)2 |
(2)请写出组合④的化学方程式H2SO4+Ba(NO3)2=BaSO4↓+2HNO3.
【实验结论】他们请教老师并讨论后知道,只有当两种化合物互相交换成分,生成物中有沉淀或水或气体生成时,复分解反应才可以发生.
【应用】写出利用熟石灰鉴别化肥氯化铵和氯化钾有关反应的化学方程式2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.
【拓展延伸】实验结束后,他们将所有废液收集在废液缸中静置,观察到白色沉淀和无色的上层清液.为了确定沉淀和清液的成分,继续展开探究.
【实验1】探究沉淀的成分.
【提出猜想】Ⅰ.沉淀只有硫酸钡Ⅱ.沉淀只有碳酸钡Ⅲ.沉淀中含有硫酸钡和碳酸钡.梅梅取少量沉淀于试管中,滴加过量的稀盐酸,观察到的现象是沉淀部分溶解,有气泡产生,证明了猜想Ⅲ是正确的.
【实验2】探究清液的成分.
①取少量清液于试管中,向其中滴加几滴硝酸钡溶液,无明显现象.
②另取少量清液于另一只试管中,滴加几滴稀硫酸,有白色沉淀产生.
【解释与结论】探究活动结束后,小组内成员通过讨论分析,一致认为清液中含有的离子除Na+、Cl-外,还有NO3-、Ba2+(指示剂除外).
【处理废液】为了防止污染环境,玲玲向废液缸中加入适量的碳酸钠溶液,对废液进行处理后,将固体回收进一步处理,溶液排放.
【交流与反思】根据你对物质溶解性的了解,结合复分解反应发生的条件,请写出一种在水溶液中一般不能发生复分解反应的可溶性盐NaNO3(写化学式).
5.小林觉得你很聪明,是他的良师益友,学完“酸的化学性质”后,邀请你与他讨论“食醋在厨房中的妙用”;
(1)复习酸的化学性质
由于小林的课堂笔记没做好,“③酸与某些金属氧化物作用”后面的化学方程式未配平,请帮他写出配平后的化学方程式:Fe2O3+6HCl=2FeCl3+3H2O
(2)讨论交流
小林自豪地说,目前世界卫生组织正在推广使用中国铁锅,使用铁锅炒菜时,放点食醋,可以补充人体需要的微量元素铁元素,该反应的原理是利用了酸的化学性质②(填序号“①”“②”或“③”).
(3)反思
盐酸、硫酸、食醋具有相似化学性质的原因是因为它们的水溶液中都有氢离子.
(1)复习酸的化学性质
| ①酸与指示剂作用 | 酸溶液能使紫色石蕊溶液变红色 | 酸溶液不能使无色酚酞溶液变色 |
| ②酸与活泼金属作用 | Fe+2HCl=FeCl2+H2↑ | Fe+H2SO4=FeSO4+H2↑ |
| ③酸与某些金属氧化物作用 | Fe2O3+HCl=FeCl3+H2O | … |
| ④… |
(2)讨论交流
小林自豪地说,目前世界卫生组织正在推广使用中国铁锅,使用铁锅炒菜时,放点食醋,可以补充人体需要的微量元素铁元素,该反应的原理是利用了酸的化学性质②(填序号“①”“②”或“③”).
(3)反思
盐酸、硫酸、食醋具有相似化学性质的原因是因为它们的水溶液中都有氢离子.
 测定空气中氧气体积分数的实验装置如图所示,在集气瓶内加入少量的水,并五等分水面以上的容积,做上记号.用弹簧夹夹紧乳胶管,点燃燃烧匙内稍过量的红磷后,立即伸入瓶中并把塞子塞紧,看到的现象是①红磷燃烧,冒出大量的白烟;
测定空气中氧气体积分数的实验装置如图所示,在集气瓶内加入少量的水,并五等分水面以上的容积,做上记号.用弹簧夹夹紧乳胶管,点燃燃烧匙内稍过量的红磷后,立即伸入瓶中并把塞子塞紧,看到的现象是①红磷燃烧,冒出大量的白烟;
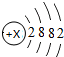 探究元素周期表可寻得一些规律.如图是一些元素的原子结构示意图.例:碳原子结构示意图的意思:6C表示6号元素碳,
探究元素周期表可寻得一些规律.如图是一些元素的原子结构示意图.例:碳原子结构示意图的意思:6C表示6号元素碳,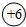 表示核内带6个单位正电荷,
表示核内带6个单位正电荷,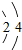 表示核外有6个电子,分两层排布,通常最外层电子数为8时较稳定.
表示核外有6个电子,分两层排布,通常最外层电子数为8时较稳定.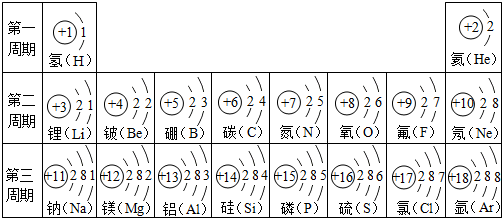
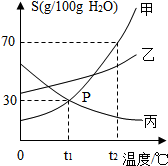 如图是甲、乙、丙三种物质(其晶体均不含结晶水)的溶解度曲线.据图回答:
如图是甲、乙、丙三种物质(其晶体均不含结晶水)的溶解度曲线.据图回答: