题目内容
5.2016年3月22日是第二十四届“世界水日”,3月22日-28日是第二十九届“中国水周”.联合国确定2016年“世界水日”的宣传主题是“水与就业”.下列措施不正确的是( )| A. | 对雨水和微咸水的收集、开发、利用和对海水的利用、淡化 | |
| B. | 洗菜时总是把泥土先抖干净再清洗 | |
| C. | 关闭巢湖流域所有化工厂 | |
| D. | 增加循环用水次数 |
分析 A.根据节约用水的要求来分析;
B.根据便于清洗进行分析分析;
C.根据工业废水处理达标后再排放进行分析;
D.根据节约用水的措施进行分析.
解答 解:A.对雨水和微咸水的收集、开发、利用和对海水的利用、淡化,达到了节水的目的,故正确;
B.洗菜时总是把泥土先抖干净后再清洗便于清洗,节约用水,故正确;
C.关闭巢湖流域所有化工厂是不现实的,工业废水可以处理达标后再排放,故错误;
D.增加循环用水次数,可以节约用水,故正确.
故选C.
点评 解答本题要充分理解保护环境的重要性,只有这样才能对相关方面的问题做出正确的判断.

练习册系列答案
相关题目
15.某实验小组的同学要探究酸碱盐中碳酸钠的化学性质,设计了如下实验装置及方案:
(一)(1)步骤①中气球变瘪的原因碳酸钠与稀盐酸反应生成CO2,内部压强大于大气压;
(2)步骤①、②可得出碳酸钠具有与盐酸反应生成CO2的性质;
(3)步骤④的操作是将注射器4稍稍向外拉,其目的是证明CO2完全被吸收;
(4)步骤⑤中发生反应的化学方程式Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
(5)步骤③④⑤可得出碳酸钠具有与含Ca2+的溶液反应生成白色沉淀的性质;
(二)上述实验结束后,实验小组的同学又对瓶内溶液的成分十分好奇,进行了探究:
(1)【提出猜想】通过分析,一致认为瓶内溶液的溶质中一定含有NaOH和NaCl,可能含有氢氧化钙或Na2CO3.
(2)【实验验证】设计实验方案确定溶液中溶质的组成.
(3)【反思与交流】根据所学化学知识,除了以上方案外,下列哪些物质可以代替试管B中加入的Na2CO3溶液完成该实验?ae(填序号)
a.K2CO3 b.BaCO3 c.CO2 d.无色酚酞 e.CuSO4.
| 实验装置 | 实验步骤及操作 | 实验现象 |
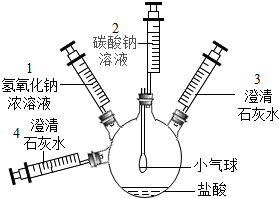 | ①将注射器2中的溶液推入盛有稀盐酸的瓶中,至不再有气泡产生. | 气球变瘪 |
| ②将注射器3稍稍向外拉 | 澄清石灰水变浑浊 | |
| ③将注射器1中的溶液推入瓶中 | 气球鼓起 | |
| ④将注射器4稍稍向外拉 | 无明显现象 | |
| ⑤将注射器4中的溶液推入瓶中 | 产生白色沉淀 |
(2)步骤①、②可得出碳酸钠具有与盐酸反应生成CO2的性质;
(3)步骤④的操作是将注射器4稍稍向外拉,其目的是证明CO2完全被吸收;
(4)步骤⑤中发生反应的化学方程式Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
(5)步骤③④⑤可得出碳酸钠具有与含Ca2+的溶液反应生成白色沉淀的性质;
(二)上述实验结束后,实验小组的同学又对瓶内溶液的成分十分好奇,进行了探究:
(1)【提出猜想】通过分析,一致认为瓶内溶液的溶质中一定含有NaOH和NaCl,可能含有氢氧化钙或Na2CO3.
(2)【实验验证】设计实验方案确定溶液中溶质的组成.
| 实验操作 | 实验现象 | 实验结论 |
| 分别取少量溶液于A、B两支试管中,A中 加入CaCl2溶液,B中加入Na2CO3溶液 | A中产生白色沉淀,B中没有沉淀 | 瓶内溶液中溶质的成分为NaOH、NaCl和Na2CO3 |
a.K2CO3 b.BaCO3 c.CO2 d.无色酚酞 e.CuSO4.
16.下列是“家庭小实验”不能达到预期目的是( )
| A. | 将铅笔芯粉末放入锁芯,使开锁更灵活 | |
| B. | 用小卵石、石英砂、活性炭等作家庭净水器 | |
| C. | 向洗净的碎鸡蛋壳中加入食盐水可制二氧化碳 | |
| D. | 用冷碟子放在蜡烛火焰上方,压住火焰,制取少量炭黑 |
13.下列关于碳和碳的氧化物的说法错误的是( )
| A. | 石墨和金刚石都是由碳原子直接构成的单质 | |
| B. | 二氧化碳可用于光合作用、灭火、人工降雨等 | |
| C. | 一氧化碳能与血液中的血红蛋白结合导致中毒 | |
| D. | 一氧化碳和二氧化碳的性质用途的差异较大,是因为组成它们的元素种类不同 |
10.已知某无色溶液中大量存在氢氧根离子、硫酸根离子和X离子,则X离子可能是( )
| A. | 钡离子 | B. | 氢离子 | C. | 钠离子 | D. | 铜离子 |
5.如图所示图象关系合理的是( )
| A. |  在久置的NaOH溶液中滴加盐酸 | |
| B. |  锌与一定质量的稀硫酸反应 | |
| C. |  向等质量的镁和氧化镁加入足量相同溶质质量分数的稀盐酸 | |
| D. |  向pH=9的NaOH溶液中不断加水 |


 图1是元素周期表中铝元素的部分信息,图2是铝原子的结构示意图,下列说法中,不正确的是B
图1是元素周期表中铝元素的部分信息,图2是铝原子的结构示意图,下列说法中,不正确的是B