题目内容
2.实验室制取氧气时,某同学取质量为x的高锰酸钾加热,记录产生氧气的质量与反应时间的关系如图1所示,请回答下列问题: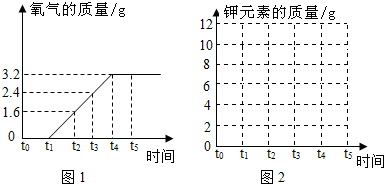
(1)t0-t1和t4-t5时段固体质量都不变,原因是否相同?否(填“是”或“否”).
(2)请在图2坐标中,画出固体中钾元素质量在t0-t5时段变化示意图.
(3)请根据图中数据计算高锰酸钾的质量x为多少?(写出计算过程)
分析 (1)根据图中信息解答;
(2)根据图1可知,氧气的质量为3.2克,根据氧气的质量,利用氧气的质量根据反应的方程式即可计算出高锰酸钾的质量;
(3)根据质量守恒定律,化学反应前后锰元素的质量不变解答.
解答 解:
(1)根据图中信息可知:t0-t1固体质量不变,是因为反应还未进行;t4-t5时固体质量不变,是因为反应进行完全.
故填:否;
(2)31.6g高锰酸钾中锰元素的质量是31.6g×$\frac{55}{158}$=11g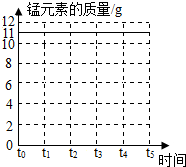
(3)设高锰酸钾的质量是x,由图象可知该反应生成的氧气质量是3.2g;
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
316 32
x 3.2g
$\frac{316}{x}$=$\frac{32}{3.2g}$,x=31.6g.
高锰酸钾的质量x为31.6g.
点评 本题为根据化学方程式计算类问题中的基础计算,完整的计算步骤、规律的书写格式是解答此类问题时需要留意的地方.

练习册系列答案
相关题目
12.我们盘锦地区使用的粗盐大多由海水为原料制得的,其中除了含有泥沙等难溶性物质外还含有一些可溶性钙镁化合物,如氯化钙,氯化镁等.几位同学想除去粗盐中难溶性杂质,并对所得精盐的成分进行研究.请你帮助他们完成设计方案:
(1)除去粗盐中难溶性杂质:操作步骤如下:①溶解,②过滤,③蒸发,④回收并计算产率.此过程中都用到的玻璃仪器是玻璃棒,它在步骤③中的作用是搅拌防止局部温度过高造成液体飞溅.
(2)在上述除杂质采用的方法中利用了氯化钠的溶于水和溶解度受温度影响较小性质.
(3)在制得的精盐中除了含有氯化钠外还含有氯化钙,氯化镁等,检验方案如下:
(1)除去粗盐中难溶性杂质:操作步骤如下:①溶解,②过滤,③蒸发,④回收并计算产率.此过程中都用到的玻璃仪器是玻璃棒,它在步骤③中的作用是搅拌防止局部温度过高造成液体飞溅.
(2)在上述除杂质采用的方法中利用了氯化钠的溶于水和溶解度受温度影响较小性质.
(3)在制得的精盐中除了含有氯化钠外还含有氯化钙,氯化镁等,检验方案如下:
| 实验目的 | 实验步骤 | 实验现象 | 实验结论 |
检验精盐中的物质 | 取少量精盐加水溶解: ①加入碳酸钠溶液; ②另取样加入氢氧化钠溶液 | 都产生 白色沉淀. | ①含有氯化钙 ②含有氯化镁 |
10.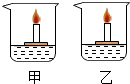 烧杯中分别盛有两种溶质不同的无色溶液,小木块上各有一支燃着的蜡烛,向甲烧杯撒入白色粉末X后,发现烧杯中蜡烛会熄灭,向乙烧杯中撒入黑色粉末Y后,则发现烧杯中蜡烛燃烧更旺.根据所学知识推测,X、Y分别是( )
烧杯中分别盛有两种溶质不同的无色溶液,小木块上各有一支燃着的蜡烛,向甲烧杯撒入白色粉末X后,发现烧杯中蜡烛会熄灭,向乙烧杯中撒入黑色粉末Y后,则发现烧杯中蜡烛燃烧更旺.根据所学知识推测,X、Y分别是( )
 烧杯中分别盛有两种溶质不同的无色溶液,小木块上各有一支燃着的蜡烛,向甲烧杯撒入白色粉末X后,发现烧杯中蜡烛会熄灭,向乙烧杯中撒入黑色粉末Y后,则发现烧杯中蜡烛燃烧更旺.根据所学知识推测,X、Y分别是( )
烧杯中分别盛有两种溶质不同的无色溶液,小木块上各有一支燃着的蜡烛,向甲烧杯撒入白色粉末X后,发现烧杯中蜡烛会熄灭,向乙烧杯中撒入黑色粉末Y后,则发现烧杯中蜡烛燃烧更旺.根据所学知识推测,X、Y分别是( )| A. | X:Al(OH)3 Y:C | B. | X:Mg Y:CuO | ||
| C. | X:Na2CO3 Y:MnO2 | D. | X:CaCO3 Y:Fe3O4 |
11.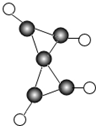 科学家最近在-100℃的低温下合成了一种化合物X,此分子的模型如图所示,其中每个
科学家最近在-100℃的低温下合成了一种化合物X,此分子的模型如图所示,其中每个 代表一个碳原子,每个
代表一个碳原子,每个 代表一个氢原子,下列说法中不正确的是( )
代表一个氢原子,下列说法中不正确的是( )
 科学家最近在-100℃的低温下合成了一种化合物X,此分子的模型如图所示,其中每个
科学家最近在-100℃的低温下合成了一种化合物X,此分子的模型如图所示,其中每个 代表一个碳原子,每个
代表一个碳原子,每个 代表一个氢原子,下列说法中不正确的是( )
代表一个氢原子,下列说法中不正确的是( )| A. | 该高分子化合物的化学式C5H4 | |
| B. | 该分子中碳元素的质量分数为93.75% | |
| C. | 该分子中的氢原子与碳原子的原子个数比为5:4 | |
| D. | 等质量的该物质与甲烷相比,甲烷燃烧时消耗的氧气更多 |
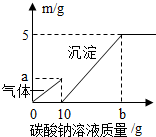 实验室用石灰石和稀盐酸制取二氧化碳后,兴趣小组同学对废液的溶质成分进行鉴定.取上层废液50g,逐滴加入质量分数为26.5%的碳酸钠溶液,开始出现气泡,滴加至10g出现白色沉淀,继续滴加至沉淀不再产生,并绘制了有关数据的图象.
实验室用石灰石和稀盐酸制取二氧化碳后,兴趣小组同学对废液的溶质成分进行鉴定.取上层废液50g,逐滴加入质量分数为26.5%的碳酸钠溶液,开始出现气泡,滴加至10g出现白色沉淀,继续滴加至沉淀不再产生,并绘制了有关数据的图象.
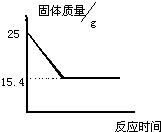 现有氯酸钾和二氧化锰的混合物,加热完全反应后,剩余固体质量与时间关系如图所示,求:
现有氯酸钾和二氧化锰的混合物,加热完全反应后,剩余固体质量与时间关系如图所示,求: