题目内容
16. 某兴趣小组同学欲探究NaOH溶液与CO2气体的反应,设计如图所示实验装置:
某兴趣小组同学欲探究NaOH溶液与CO2气体的反应,设计如图所示实验装置:(1)若导管a与b连接,将分液漏斗中的NaOH溶液注入锥形瓶,关闭分液漏斗上的活塞,振荡,然后打开导管上的活塞,观察到的实验现象是集气瓶内的水流入锥形瓶中,CO2与NaOH反应的化学方程式是2NaOH+CO2═Na2CO3+H2O;
(2)探究反应后锥形瓶内溶液中溶质的成分:
已知Na2CO3+H2O+CO2═2NaHCO3
NaHCO3+NaOH═Na2CO3+H2O
【提出猜想】Ⅰ.NaOH和Na2CO3;Ⅱ.Na2CO3;
Ⅲ.NaHCO3;Ⅳ.Na2CO3和NaHCO3.
【查阅资料】①Ca(OH)2与Na2CO3、NaHCO3均能反应且有白色沉淀生成;
②CaCl2与Na2CO3能反应且有白色沉淀生成,与NaHCO3不反应;
③NaHCO3溶液显碱性,可与酸反应生成CO2气体.
【设计实验】限选试剂:Ca(OH)2溶液、CaCl2溶液、稀盐酸、酚酞试液.
| 实验操作 | 实验现象 | 实验结论 |
| 1.取少量反应后溶液于试管中,加入足量的 氯化钙振荡 | 产生白色沉淀 | 猜想Ⅲ不成立 |
| 2.将操作Ⅰ所得混合物过滤,向滤液中加入足量的 稀盐酸,振荡 | 有气泡产生 | 猜想Ⅳ成立 |
分析 (1)根据二氧化碳和氢氧化钠反应后气压会减小,造成出现某特定的现象解答;
(2)【提出猜想】根据二氧化碳和氢氧化钠反应时,如果氢氧化钠过量,则溶质是氢氧化钠和碳酸钠;
如果二氧化碳过量,但是不能完全消耗生成的碳酸钠,则溶质是碳酸钠和碳酸氢钠;
如果氢氧化钠和二氧化碳恰好完全反应,则溶质是碳酸钠;
如果二氧化碳过量,并且把碳酸钠完全消耗,则溶质是碳酸氢钠进行分析;
【设计实验】根据①Ca(OH)2与Na2CO3、NaHCO3均能反应且有白色沉淀生成;
②CaCl2与Na2CO3能反应且有白色沉淀生成,与NaHCO3不反应;
③NaHCO3溶液显碱性,可与酸反应生成CO2气体进行分析;
【拓展应用】根据空气中的二氧化碳会与氢氧化钠反应进行分析.
解答 解:(1)二氧化碳和氢氧化钠反应后气压会减小,集气瓶内的水流入锥形瓶中,CO2与NaOH反应生成碳酸钠和水,化学方程式为:2NaOH+CO2═Na2CO3+H2O;
(2)【提出猜想】二氧化碳和氢氧化钠反应时,如果氢氧化钠过量,则溶质是氢氧化钠和碳酸钠;
如果二氧化碳过量,但是不能完全消耗生成的碳酸钠,则溶质是碳酸钠和碳酸氢钠;
如果氢氧化钠和二氧化碳恰好完全反应,则溶质是碳酸钠;
如果二氧化碳过量,并且把碳酸钠完全消耗,则溶质是碳酸氢钠,所以猜想II是Na2CO3;
因二氧化碳不但能跟氢氧化钠反应,二氧化碳还能溶于水也跟水反应.所以让人产生质疑;
【设计实验】
| 实验操作 | 实验现象 | 实验结论 |
| 1.取少量反应后溶液于试管中,加入足量的氯化钙振荡 | 产生白色沉淀 | 猜想Ⅲ不成立 |
| 2.将操作Ⅰ所得混合物过滤,向滤液中加入足量的稀盐酸,振荡 | 有气泡产生 | 猜想Ⅳ成立 |
故答案为:(1)烧杯内的水流入锥形瓶中,2NaOH+CO2═Na2CO3+H2O;
(2)【提出猜想】Na2CO3;
【设计实验】
| 实验操作 | 实验现象 | 实验结论 |
| 1.氯化钙 | 产生白色沉淀 | |
| 2.稀盐酸 | 有气泡产生 |
点评 实验方案的设计和评价,是素质教育对化学实验教学的能力培养目标之一,而能力的考查又逐渐成了中考重点和热点,但是,该内容也是学习难点,应重点练习,养成对实验进行评价我自我设计实验的习惯.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.分类是化学学习的重要方法,下列分类不正确的是( )
| A. | 有机物:甲烷、二氧化碳 | B. | 盐类:小苏打、纯碱 | ||
| C. | 氮肥:氯化铵、尿素 | D. | 混合物:空气、自来水 |
7.下列物质的用途主要利用其物理性质的是( )
| A. | NaHCO3治疗胃酸过多 | B. | 用干冰进行人工降雨 | ||
| C. | 用熟石灰改良酸性土壤 | D. | 用指示剂测定溶液的酸碱性 |
4.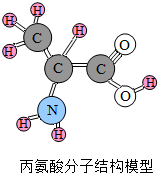 蛋白质是由多种氨基酸构成的化合物,丙氨酸是其中的一种,化学式为C3H7NO2,下列有关丙氨酸的叙述不正确的是( )
蛋白质是由多种氨基酸构成的化合物,丙氨酸是其中的一种,化学式为C3H7NO2,下列有关丙氨酸的叙述不正确的是( )
 蛋白质是由多种氨基酸构成的化合物,丙氨酸是其中的一种,化学式为C3H7NO2,下列有关丙氨酸的叙述不正确的是( )
蛋白质是由多种氨基酸构成的化合物,丙氨酸是其中的一种,化学式为C3H7NO2,下列有关丙氨酸的叙述不正确的是( )| A. | 丙氨酸中含有碳、氢、氧、氮四种原子 | |
| B. | 一个丙氨酸分子中含有89个质子数 | |
| C. | 丙氨酸分子中氮原子和氢原子的原子个数比为1:7 | |
| D. | 丙氨酸是一种有机物 |
11.下列化学用语,书写正确的是( )
| A. | 氧化铁 FeO | B. | 氯化锌 ZnCl | ||
| C. | 硫酸根离子 SO4 | D. | 氨中氮元素的化合价$\stackrel{-3}{N}$H3 |
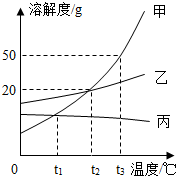 甲、乙、丙三种固体物质的溶解度曲线如图所示.据图回答问题:
甲、乙、丙三种固体物质的溶解度曲线如图所示.据图回答问题: