题目内容
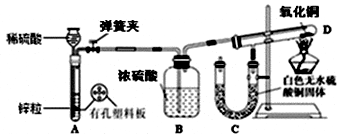
19.钠(Na)是一种非常活泼的金属,常温下能与O2、H2O等物质反应,加热时能与CO2反应生成C、CO、Na2O和Na2CO3四种物质,其中Na2O是白色固体,遇水可生成NaOH.下列有关说法不正确的是( )| A. | 钠应密封保存 | |
| B. | 钠与CO2的反应需在通风厨中进行 | |
| C. | 金属钠引起的着火可用二氧化碳灭火器灭火 | |
| D. | 钠与CO2反应生成的白色固体加水溶解后,滴加少量盐酸不会产生气泡 |
分析 A、根据题意,钠(Na)是一种非常活泼的金属,常温下能与O2、H2O等物质反应,进行分析判断.
B、根据题意,加热时能与CO2反应生成C、CO、Na2O和Na2CO3四种物质,进行分析判断.
C、根据钠能与二氧化碳反应,进行分析判断.
D、根据钠与CO2反应生成的白色固体中含有Na2O、碳酸钠,Na2O是白色固体,遇水可生成NaOH,进行分析判断.
解答 解:A、钠(Na)是一种非常活泼的金属,常温下能与O2、H2O等物质反应,钠应密封保存,故选项说法正确.
B、加热时能与CO2反应生成C、CO、Na2O和Na2CO3四种物质,生成的一氧化碳有毒,钠与CO2的反应需在通风厨中进行,故选项说法正确.
C、钠能与二氧化碳反应,金属钠引起的着火不能用二氧化碳灭火器灭火,故选项说法错误.
D、钠与CO2反应生成的白色固体中含有碳酸钠,Na2O是白色固体,遇水可生成NaOH,加水溶解后,得到的溶液是氢氧化钠和碳酸钠的混合溶液,氢氧化钠先与稀盐酸反应,故滴加少量盐酸,不会产生气泡,故选项说法正确.
故选:C.
点评 本题难度不大,理解钠常温下能与O2、H2O等物质反应、加热时能与CO2反应,熟练掌握盐的化学性质、一氧化碳有毒等是正确解答本题的关键.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
10.下列关于物质性质和用途的因果关系描述中,不正确的是( )
| 物质及其性质 | 用途 | |
| A | N2通常情况下不易发生化学变化 | 填充食品袋防腐 |
| B | 浓硫酸具有吸水性 | 用于干燥CO2气体 |
| C | CO2密度比空气大 | 用于人工降雨 |
| D | 氨水(NH3•H2O)具有碱性 | 用于减轻蚊虫叮咬引起的痛痒 |
| A. | A | B. | B | C. | C | D. | D |
7.打火机的主要燃料是丁烷(C4H10),有关于丁烷的说法不正确的是( )
| A. | 具有可燃性 | |
| B. | 完全燃烧只生成水 | |
| C. | 碳、氢元素的质量比为24:5 | |
| D. | 一个分子由4个碳原子和10个氢原子构成 |
14.用含杂质(杂质不与酸反应)的铁10克与50克稀硫酸充分反应,铁消耗完.滤去杂质,溶液的质量为55.4克.则生成氢气的质量为( )
| A. | 0.2g | B. | 0.4g | C. | 1g | D. | 4.6g |
4.如图就金属与盐酸反应的探究实验.下列说法错误的是( )


| A. | 甲可能是Mg | |
| B. | 丁说,我是黄铜,我不怕酸 | |
| C. | 将乙放在丙的盐溶液中可以置换出丙 | |
| D. | 四种金属的活动性顺序是:甲>乙>丙>丁 |
16.化学学习中经常会遇到一些“相等”,下列有关“相等”的说法中错误的是( )
| A. | 化学反应前后原子的总数一定相等 | |
| B. | 催化剂在反应前后质量一定相等 | |
| C. | 中和反应中参加反应的酸和碱的质量一定相等 | |
| D. | 溶液稀释前后溶质的质量一定相等 |
17.化学兴趣小组同学进行如下实验与探究活动,请你参与.
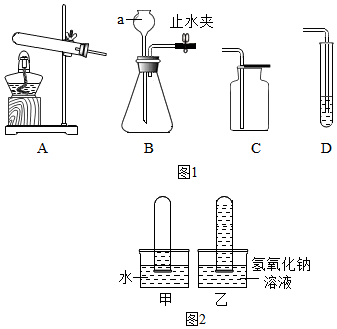
Ⅰ、制取气体并验证气体性质.(如图1所示)
(1)写出标号a仪器的名称:长颈漏斗.
(2)用A装置制取氧气,反应的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.装置C可以收集氧气,这是因为氧气具有氧气密度比空气大性质.
(3)用装置B与D组合制取并验证二氧化碳的某些性质.
①检查装置B的气密性的方法是关闭止水夹,向长颈漏斗注入一定量的水,如果长颈漏斗中会形成一段稳定的水柱,说明装置气密性良好.
②装置D中若盛放滴有紫色石蕊试液的水,可以观察到的现象是紫色石蕊溶液变红色;若盛放氢氧化钠溶液,则没有明显现象产生.
Ⅱ、在老师的指导下,兴趣小组同学多角度探究二氧化碳与氢氧化钠确实能发生化学反应.
(4)小明进行如下实验:将收集满二氧化碳的两支试管(相同规格)分别倒立在水和氢氧化钠溶液中,轻轻晃动试管,产生了如图2所示现象.
①小明根据乙试管内的液体比甲试管内的液体高得多,判断二氧化碳和氢氧化钠发生了反应,反应的化学方程式为2NaOH+CO2=Na2CO3+H2O.
②甲实验的目的是对比实验.
(5)小菁取氢氧化钠溶液于烧杯中,用pH计测定溶液的pH为13.5.往溶液中通入二氧化碳一会儿,测得溶液的pH为11.2,继续通入二氧化碳,再测得溶液的pH为9.2,溶液的pH降低的原因是溶液中氢氧化钠减少,溶液碱性减弱,该实验可以说明二氧化碳和氢氧化钠发生了反应.
(6)请你根据化学变化的本质特征,设计另一个实验方案:

Ⅰ、制取气体并验证气体性质.(如图1所示)
(1)写出标号a仪器的名称:长颈漏斗.
(2)用A装置制取氧气,反应的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.装置C可以收集氧气,这是因为氧气具有氧气密度比空气大性质.
(3)用装置B与D组合制取并验证二氧化碳的某些性质.
①检查装置B的气密性的方法是关闭止水夹,向长颈漏斗注入一定量的水,如果长颈漏斗中会形成一段稳定的水柱,说明装置气密性良好.
②装置D中若盛放滴有紫色石蕊试液的水,可以观察到的现象是紫色石蕊溶液变红色;若盛放氢氧化钠溶液,则没有明显现象产生.
Ⅱ、在老师的指导下,兴趣小组同学多角度探究二氧化碳与氢氧化钠确实能发生化学反应.
(4)小明进行如下实验:将收集满二氧化碳的两支试管(相同规格)分别倒立在水和氢氧化钠溶液中,轻轻晃动试管,产生了如图2所示现象.
①小明根据乙试管内的液体比甲试管内的液体高得多,判断二氧化碳和氢氧化钠发生了反应,反应的化学方程式为2NaOH+CO2=Na2CO3+H2O.
②甲实验的目的是对比实验.
(5)小菁取氢氧化钠溶液于烧杯中,用pH计测定溶液的pH为13.5.往溶液中通入二氧化碳一会儿,测得溶液的pH为11.2,继续通入二氧化碳,再测得溶液的pH为9.2,溶液的pH降低的原因是溶液中氢氧化钠减少,溶液碱性减弱,该实验可以说明二氧化碳和氢氧化钠发生了反应.
(6)请你根据化学变化的本质特征,设计另一个实验方案:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量氢氧化钠溶液于试管中,通入一定量二氧化碳后,再向溶液中滴加稀盐酸 | 有大量气泡冒出 | 二氧化碳与氢氧化钠发生了化学反应 |