题目内容
 某兴趣小组的同学在化学实验室发现一瓶盛有无色溶液的试剂瓶,其标签部分破损(如图所示).
某兴趣小组的同学在化学实验室发现一瓶盛有无色溶液的试剂瓶,其标签部分破损(如图所示).【观察与问题】这瓶溶液是什么呢?同学们展开了探究.
【假设与预测】假设一:这瓶溶液是H2SO4
假设二:这瓶溶液是CuSO4
假设三:这瓶溶液是Na2SO4等硫酸盐溶液
【实验与事实】表达与交流】同学们经过讨论,很快排除了假设二,因为
【实验与事实】
(1)用
(2)取少量该溶液与试管中,加入金属锌粒,观察到有气泡产生,该气体由
(3)取少量该溶液与试管中,加入Na2CO3溶液,也观察到有大量气泡产生,则该反应的化学方程式为
【解释与结论】通过以上实验探究,确认该瓶溶液为硫酸.
【拓展与迁移】通过以上探究活动,兴趣小组的同学总结出了两条酸的化学性质,如:
酸+金属═盐+氢气
酸+盐═新酸+新盐
请你用化学方程式表示酸的另外一条化学性质
考点:缺失标签的药品成分的探究,酸的化学性质,盐的化学性质
专题:科学探究
分析:根据硫酸铜溶液的颜色来分析;硫酸是一种强酸,根据实验猜想气体是氢气,根据氢气的结构来分析;根据硫酸与碳酸钠反应的过程来书写;结合酸的通性来分析.
解答:解:硫酸铜溶液是蓝色,故不可能是硫酸铜溶液;故填:硫酸铜溶液是蓝色的;
【实验与事实】
(1)用pH试纸来测定溶液的酸碱度,若为强酸性则为硫酸;故填:pH试纸;
(2)锌与酸反应释放出氢气,氢气是由氢分子构成的,故填:分子;
(3)稀硫酸与碳酸钠反应生成硫酸钠、水和二氧化碳;故填:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑;
【拓展与迁移】酸具有很多通性,如酸与碱发生中和反应生成盐和水.故填:2NaOH+H2SO4=Na2SO4+2H2O.(答案合理即可)
【实验与事实】
(1)用pH试纸来测定溶液的酸碱度,若为强酸性则为硫酸;故填:pH试纸;
(2)锌与酸反应释放出氢气,氢气是由氢分子构成的,故填:分子;
(3)稀硫酸与碳酸钠反应生成硫酸钠、水和二氧化碳;故填:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑;
【拓展与迁移】酸具有很多通性,如酸与碱发生中和反应生成盐和水.故填:2NaOH+H2SO4=Na2SO4+2H2O.(答案合理即可)
点评:本题考查缺失标签的药品成分的探究,属于开放性习题,能较好的考查学生的实验探究能力,实验设计过程,训练学生思维,体现学生应用知识知识解决问题的能力.

练习册系列答案
 每课必练系列答案
每课必练系列答案
相关题目
下列变化属于物理变化的是( )
A、 小苏打制汽水 |
B、 氢氧化钠制叶脉书签 |
C、 侯德榜联合制碱 |
D、 积雪用氯化钠来消除 |
在一个密闭容器中放入W、G、H、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表:关于此反应的认识不正确的是( )
| 物质 | W | G | H | P |
| 反应前质量/g | 18 | 1 | 2 | 32 |
| 反应后质量/g | 待测 | 26 | 2 | 12 |
| A、物质H一定是该反应的催化剂 |
| B、该反应一定是化合反应 |
| C、W、P是反应物 |
| D、待测值为13 |
如图是元素周期表中第三周期元素的原子结构示意图:
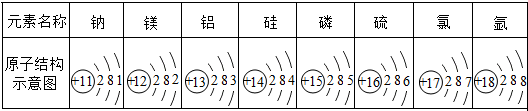
依据如图判断,下列结论正确的是( )

依据如图判断,下列结论正确的是( )
| A、12 号元素的原子,在化学反应中容易得到电子变成离子 |
| B、钠元素与硫元素形成化合物的化学式为Na2S |
| C、第三周期元素的化学性质相似 |
| D、Cl→Cl-,则 Cl 核内有 18 个质子 |
在一定温度下,氯化钠的溶解度为a,这时该溶液中溶质的质量分数为b%,a与b的大小关系是( )
| A、a<b | B、a>b |
| C、a﹦b | D、无法确定 |

