题目内容
9.小明家有一瓶标签破损的钙片,为测定钙片中碳酸钙的质量分数,小明做了如下研究,取12g钙片,放入100g稀盐酸质量分数为7.3%中.待完全反应后.测得剩余物质的总质量为107.6g求:(1)二氧化碳的质量(2)碳酸钙的质量分数.分析 钙片中的碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,12g钙片含有其它物质,不是纯净物的质量;由于题目为说明100g稀盐酸质量分数为7.3%是否恰好完全反应,故不要用稀盐酸的质量进行计算;由质量守恒定律,混合物减少的质量即为生成二氧化碳气体的质量,由反应的化学方程式列式计算出参加反应的碳酸钙的质量,进而计算出碳酸钙的质量分数.
解答 解:(1)由质量守恒定律,生成二氧化碳的质量为12g+100g-107.6g=4.4g.
(2)设参加反应的碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 4.4g
$\frac{100}{44}=\frac{x}{4.4g}$ x=10g
碳酸钙的质量分数为$\frac{10g}{12g}×$100%≈83.3%.
答:(1)二氧化碳的质量为4.4g;(2)碳酸钙的质量分数为83.3%.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出二氧化碳的质量是正确解答本题的前提和关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.同学们在做氧气性质实验时,将点燃的木炭伸人集气瓶内,有的现象明显,有的却不明显.导致现象不明显的原因可能是( )
| A. | 排水法收集时未将气体收集满,底部留有少量的水 | |
| B. | 导管口有气泡冒出开始收集氧气 | |
| C. | 收集满后盖上毛玻璃片拿出水面 | |
| D. | 收集满氧气的集气瓶正放于桌面 |
10.医院给病人输氧时用到类似如图所示的装置.关于该装置,下列说法不正确的是( )
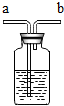

| A. | 实验室中将该装置装满水收集氧气时,气体从b导管进入 | |
| B. | 实验室中将该装置盛浓硫酸干燥氧气时,气体从b导管进入 | |
| C. | 输氧时,a导管连接供给氧气的钢瓶 | |
| D. | 输氧时,该装置也能用来观测氧气输出的速率. |
 人类的日常生活和工、农业生产都离不开水.请回答下列与水有关的问题:
人类的日常生活和工、农业生产都离不开水.请回答下列与水有关的问题:

