题目内容
20.同学们在做氧气性质实验时,将点燃的木炭伸人集气瓶内,有的现象明显,有的却不明显.导致现象不明显的原因可能是( )| A. | 排水法收集时未将气体收集满,底部留有少量的水 | |
| B. | 导管口有气泡冒出开始收集氧气 | |
| C. | 收集满后盖上毛玻璃片拿出水面 | |
| D. | 收集满氧气的集气瓶正放于桌面 |
分析 根据题意:将点燃的木炭伸入集气瓶内,有的现象明显,有的不明显,导致现象不明显的原因可能是收集的氧气不纯,混入空气,然后结合排水法收集氧气的注意事项分析解答.
解答 解:将点燃的木炭伸入集气瓶内,有的现象明显,有的不明显,导致现象不明显的原因可能是收集的氧气不纯,混入空气;
A、排水法收集结束时集气瓶内有水,不妨碍氧气的纯度,不符合题意;
B、导管口开始出来的气体是试管内的空气,所以要等连续放出气泡时开始收集,符合题意;
C、排水法收集满后在水下盖上毛玻璃片拿出水面,不会混入空气,不符合题意;
D、氧气的密度比空气大,收集满氧气的集气瓶正放于桌面,氧气不会逸出,不符合题意;
故选:B.
点评 本题考查了对实验现象的正确分析和对排水法收集氧气的考查,掌握相关知识即可正确解答,难度不大.

练习册系列答案
相关题目
11.请根据如图回答问题:
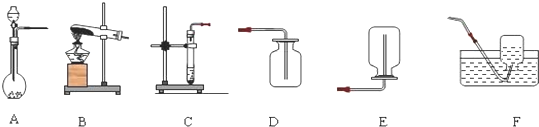
(1)实验室用高锰酸钾制取氧气,应选用的发生装置是B,写出用高锰酸钾制取氧气反应的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(2)实验室里常用大理石(或石灰石)和稀盐酸在常温下反应制取二氧化碳,可选用的气体发生装置是A(或C).请写出实验室制取二氧化碳反应的化学方程式CaC03+2HCl═CaCl2+H20+C02↑.
(2)实验室里可用氢氧化钙与氯化铵的固体混合物加热制取氨气,则制取氨气所需的气体发生装置为B,氨气极易溶于水,一般可用E装置收集氨气.
(3)石灰厂为了测定一批石灰石样品中碳酸钙的质量分数,取用4g石灰石样品,把20g稀盐酸分4次加人样品中(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如下表:
①该石灰石样品中碳酸钙的质量分数是75%;
②计算 该石灰石样品完全反应后生成二氧化碳的总质量是多少?(写计算过程)

(1)实验室用高锰酸钾制取氧气,应选用的发生装置是B,写出用高锰酸钾制取氧气反应的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(2)实验室里常用大理石(或石灰石)和稀盐酸在常温下反应制取二氧化碳,可选用的气体发生装置是A(或C).请写出实验室制取二氧化碳反应的化学方程式CaC03+2HCl═CaCl2+H20+C02↑.
(2)实验室里可用氢氧化钙与氯化铵的固体混合物加热制取氨气,则制取氨气所需的气体发生装置为B,氨气极易溶于水,一般可用E装置收集氨气.
(3)石灰厂为了测定一批石灰石样品中碳酸钙的质量分数,取用4g石灰石样品,把20g稀盐酸分4次加人样品中(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如下表:
| 稀盐酸的用量 | 第一次加入5g | 第二次加入5g | 第三次加入5g | 第四次加人5g |
| 剩余固体的质量 | 3g | 2g | l g | 1g |
②计算 该石灰石样品完全反应后生成二氧化碳的总质量是多少?(写计算过程)
15.下列现象的描述错误的是( )
| A. | 木炭在氧气中燃烧发出白光 | |
| B. | 铁丝在氧气中燃烧剧烈,火星四射,生成黑色固体 | |
| C. | 铜丝在空气中加热变黑 | |
| D. | 铁插入稀硫酸中溶液产生气泡,溶液变成蓝色 |
 如图是A、B、C三种固体物质的溶解度曲线,试看图后回答:
如图是A、B、C三种固体物质的溶解度曲线,试看图后回答: