题目内容
5.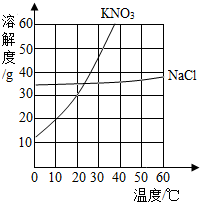 如图是KNO3和NaCl溶解度曲线,根据如图所指,回答下列问题
如图是KNO3和NaCl溶解度曲线,根据如图所指,回答下列问题(1)30℃时KNO3的溶解度比NaCl的溶解度大
(2)20℃时,100g水中加入10g KNO3,将其转化为该温度的饱和溶液,需加入KNO3质量约20g
(3)除去KNO3中含有的少量NaCl;先将混合物配成高温的饱和溶液,然后降温结晶,过滤得到KNO3固体.
分析 根据已有的溶解度曲线的意义进行分析解答,根据溶解度曲线可以比较在同一温度下二者的溶解度大小,根据溶解度确定溶质的质量;根据析出晶体的方法解答.
解答 解:(1)据图可以看出,30℃时KNO3的溶解度比NaCl的溶解度大,故填:大;
(2)20℃时,硝酸钾的溶解度为30g,100g水中加入10g KNO3,将其转化为该温度的饱和溶液,需加入KNO3质量20g,故填;20; (3)硝酸钾的溶解度随温度升高变化明显,故除去KNO3中含有的少量NaCl;先将混合物配成高温的饱和溶液,然后降温结晶,故填:降温结晶.
点评 本题考查溶解度曲线的意义及应用,根据溶解度曲线可判断饱和溶液与不饱和溶液转化的方法,对于溶解度随温度升高而增大的物质,由不饱和溶液变成饱和溶液只能是降温,本考点主要出现在选择题和填空题中.

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案
相关题目
16. 某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象,如图所示,下列说法错误的是( )
某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象,如图所示,下列说法错误的是( )
 某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象,如图所示,下列说法错误的是( )
某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象,如图所示,下列说法错误的是( )| A. | 图中c点所示溶液呈酸性 | |
| B. | 图中a点所示溶液中,含有的溶质是Na2SO4和H2SO4 | |
| C. | 该实验是将硫酸逐滴滴入到盛有氢氧化钠溶液的烧杯中 | |
| D. | 由a点到b点的pH变化过程证明酸和碱发生了中和反应 |
13.下列变化中属于化学变化的是( )
| A. | 水的沸腾 | B. | 蜡烛燃烧 | C. | 研碎胆矾 | D. | 干冰升华 |
20.在CaCO3→CaO→Ca(OH)2→NaOH的各步转化中发生的反应,不包括下列哪种类型( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
14.北京奥运会期间对大量盆裁鲜花使用了S--诱抗素制剂,以保持鲜花的盛开.S--诱抗素的化学式为C15H20O4,下列有关S--诱抗素的叙述中错误的是( )
| A. | S--诱抗素由三种元素组成 | |
| B. | S--诱抗素属于有机物 | |
| C. | S--诱抗素中碳、氢、氧三种元素的质量比为45:5:16 | |
| D. | S--诱抗素中含有15个氢原子 |
15.下列化学实验中能达到预期实验结果的是( )
| A. | 将100g 10%的稀盐酸加热蒸发掉50g水,能得到质量分数为20%的盐酸 | |
| B. | 用普通的pH试纸测定某未知溶液的pH为5.5 | |
| C. | 20℃时,可配制出10%的氢氧化钙溶液 | |
| D. | 用湿润的红色石蕊试纸检验某气体是否为氨气 |

 分析甲、乙两种固体的溶解度曲线,回答下列问题
分析甲、乙两种固体的溶解度曲线,回答下列问题