题目内容
10.一瓶空气中久置的氢氧化钠固体,为探究其成分,取少量该样品溶于水分别进行如图实验: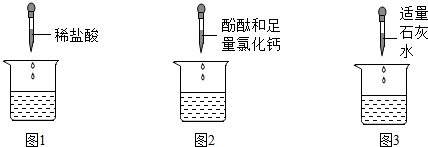
(1)图1中,加入足量盐酸后,产生气泡说明氢氧化钠样品中含有Na2CO3.
(2)图2实验,经检验氢氧化钠部分变质,则观察到的现象是有白色沉淀产生且溶液变红.
(3)图3实验,可除去氢氧化钠中变质产生的杂质,发生反应的化学方程式表示为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
(4)实验后经三个烧杯中得到的溶液和上层清液倒入同一容器内,充分混合后只得到红色溶液.分析溶液中离子存在情况为一定有Na+、Cl-、OH-,可能有Ca2+.
分析 (1)根据碳酸钠的性质来分析;
(2)氢氧化钠部分变质,也就是既有氢氧化钠,也有碳酸钠;
(3)可用氢氧化钙溶液来除杂质;
(4)根据反应的过程来分析.
解答 解:(1)氢氧化钠与盐酸反应生成氯化钠和水,碳酸钠与稀盐酸反应生成氯化钠、水和二氧化碳,加入稀盐酸有气泡产生,说明氢氧化钠变质生成了碳酸钠;故填:Na2CO3;
(2)碳酸钠能与氯化钙溶液反应生成碳酸钙白色沉淀和氯化钠,氯化钙和氯化钠溶液均显中性,若无色的酚酞试液变红色,则说明溶液中含存在氢氧化钠;故填:
有白色沉淀产生且溶液变红;
(3)加入适量的氢氧化钙溶液,直到不再产生沉淀为止,氢氧化钙与碳酸钠反应生成碳酸钙白色沉淀和氢氧化钠,故填:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
(4)氢氧化钠、碳酸钠与稀盐酸反应均生成氯化钠,溶液变红,说明溶液显碱性,含有氢氧根离子,还可能由于氯化钙过量而含有钙离子;故填:一定有Na+、Cl-、OH-,可能有Ca2+.
点评 本题综合利用了物质的组成、溶液的酸碱性及物质的变化规律对未知物质进行鉴别,体现运用化学知识分析问题、解决问题的能力.

练习册系列答案
相关题目
18.下列实验方法错误的是( )
| A. | 用点燃法区分CO和CO2 | B. | 用煮沸的方法鉴别软水和硬水 | ||
| C. | 用燃烧的方法鉴别羊毛和涤纶 | D. | 用互相刻画的方法比较金属的硬度 |
15.分析推理是化学学习中常用的思维方法,下列说法正确的是( )
| A. | 离子都带有电荷,所以带有电荷的粒子一定是离子 | |
| B. | 溶液具有均一、稳定的特征,所以均一、稳定的液体一定是溶液 | |
| C. | 单质中只含有一种元素,所以由一种元素组成的纯净物一定是单质 | |
| D. | 复分解反应中有沉淀或气体或水生成,所以生成其一的反应一定是复分解反应 |
 在盐酸、碳酸钠、火碱、二氧化碳、镁、食盐、石灰水、氧化剂、银、木炭粉等物质中,按类别选择适当物质,使如图连线的物质之间能相互反应,并回答问题:
在盐酸、碳酸钠、火碱、二氧化碳、镁、食盐、石灰水、氧化剂、银、木炭粉等物质中,按类别选择适当物质,使如图连线的物质之间能相互反应,并回答问题: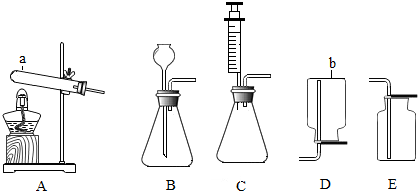
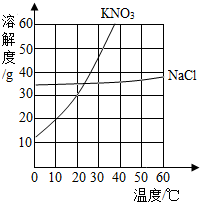 如图是KNO3和NaCl溶解度曲线,根据如图所指,回答下列问题
如图是KNO3和NaCl溶解度曲线,根据如图所指,回答下列问题