题目内容
6.回答下列问题:①海沙是由石英和贝壳小碎片组成,石英的主要成分是(用化学符号表示,下同)SiO2,贝壳的主要成分是CaCO3.
②请写出一种同时符合下列两个条件的化合物的名称是氢氧化钙,化学式Ca(OH)2.
(1)由氧、硅、氢、碳、钙五种元素中的三种组成;
(2)按组成分类,与①中两种物质的主要成分类型不同.
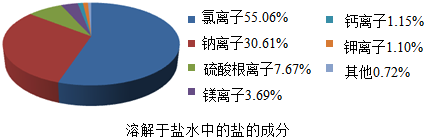
③海水中含有多种无机盐,各离子的含量如图所示,其中由硫酸根离子和镁离子构成盐的化学式是MgSO4.
假设海水中无机盐的含量为 3.5%.钾离子全部以氯化钾的形式存在,则Wg水中含有氯化钾质量的计算公式为$\frac{Wg×3.5%×1.10%×74.5}{39}$.
④各地海水中盐的含量并不完全相同,在长江入海口处,海水中盐的含量较低,原因是河水中的淡水将海水中的盐分稀释.
⑤食用低钠盐可预防高血压,低钠盐是在氯化钠中添加了适量的氯化钾,氯化钾除了有咸味外,还带有苦味,从物质构成的角度看,氯化钾有苦味可能是钾离子造成的.
分析 ①根据石英砂的主要成分是二氧化硅,贝壳的主要成分是碳酸钙进行分析;
②根据提供的元素和物质的类别来确定物质的化学式;
③根据溶质的质量=溶液的质量×溶液中溶质的质量分数来计算;
④根据入海的河水含盐量较低进行分析;
⑤根据氯化钠和氯化钾的构成异同点进行分析.
解答 解:①石英砂的主要成分是二氧化硅,贝壳的主要成分是碳酸钙;故填:SiO2;CaCO3;
②上述两种物质分属于氧化物和盐,根据提供的元素可以组成的符合两个条件的是氢氧化钙.故填:氢氧化钙或Ca(OH)2;
③镁离子带2个单位的正电荷,硫酸根离子带2个单位的负电荷,故硫酸镁的化学式为:MgSO4,Wg海水中含有钾离子的质量为:Wg×3.5%×1.10%,那么氯化钾的质量为$\frac{Wg×3.5%×1.10%}{\frac{39}{74.5}}$.故填:MgSO4;$\frac{Wg×3.5%×1.10%×74.5}{39}$;
④在河流的入海口处,有大量的河水注入海洋,相对于海水来讲,注入海洋的河流属于淡水.所以注入海洋的河水,等于是增加了入海口处海水中的水(溶剂),造成该处海水盐的浓度降低;故填:河水中的淡水将海水中的盐分稀释;
⑤氯化钠是由钠离子和氯离子构成的,没有苦味,氯化钾是由钾离子和氯离子构成的,有苦味,据此分析可能是钾离子导致氯化钾具有苦味的;故填:钾离子.
点评 本题难度不大,掌握常见化学用语(元素符号、化学式、化合价、离子符号等)的书写方法等是正确解答此类题的关键.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
5.下列实验正确的是( )
| A. |  灭火焰 | B. |  闻气味 | C. |  读体积 | D. |  测水温 |
14.下列实验操作中,正确的是( )
| A. |  检查装置气密性 | B. |  除去CO中水蒸气 | C. |  测定溶液pH | D. |  稀释浓硫酸 |
11.物质甲是一种重要的化工原料,在点燃条件下可以和乙反应生成丙和丁.根据如图所示微观示意图得出的结论中,正确的是( )


| A. | 乙、丙、丁都是氧化物 | B. | 反应前后分子总数不变 | ||
| C. | 该反应是吸热反应 | D. | 反应中乙和丁的质量比是24:9 |
18.下列认识或说法中,正确的是( )
| A. | 向某固体中加入稀盐酸有气泡产生,可证明该物质中一定含有CO32- | |
| B. | 常温下可用Fe与AgCl反应制取Ag | |
| C. | 可用过量的Cu(OH)2除去CuSO4溶液中少量的H2SO4 | |
| D. | 将Fe(OH)3加入到滴有酚酞试液的蒸馏水中,溶液显红色 |
16.分类是学习和研究化学的常用方法.下列分类中正确的是( )
| A. | 有机物:甲烷、乙醇、葡萄糖 | |
| B. | 复合肥料:KNO3、K2CO3、(NH4)2HPO4 | |
| C. | 混合物:煤、石油、冰水共存物 | |
| D. | 三大合成材料:合金、合成纤维、合成橡胶 |
 2015年中国航空业高速发展.先进无人机亮相国庆阅兵式,首架大飞机C919总装下线.
2015年中国航空业高速发展.先进无人机亮相国庆阅兵式,首架大飞机C919总装下线.



