题目内容
14.把6克碳在24克氧气中充分燃烧,生成二氧化碳的质量是( )| A. | 30克 | B. | 22克 | C. | 32克 | D. | 44克 |
分析 根据化学方程式由碳的质量可计算出生成二氧化碳的质量.碳与氧气反应时质量比是3:8,则可知反应时氧气有剩余.
解答 解:假设6克碳充分燃烧消耗的氧气为w
C+O2 $\frac{\underline{\;点燃\;}}{\;}$CO2
12 32
6g w
$\frac{12}{6g}=\frac{32}{w}$
w=16g
说明充分燃烧后氧气有剩余,所以按碳计算二氧化碳的质量.
设生成二氧化碳的质量为x.
C+O2 $\frac{\underline{\;点燃\;}}{\;}$CO2
12 44
6g x
$\frac{12}{6g}=\frac{44}{x}$,
x=22g
故选B.
点评 此题是对化学方程式计算的考查,解题的关键是首先判断哪种物质过量,然后利用化学方程式计算即可.

练习册系列答案
相关题目
9.下列性质中,不属于水的物理性质的是( )
| A. | 纯净的水是无色、无味的透明液体 | |
| B. | 在1000℃以上,水蒸气可以分解成氢气和氧气 | |
| C. | 在标准大气压下,水在0℃时能结成冰 | |
| D. | 水是一种良好的溶剂,能溶解多种物质 |

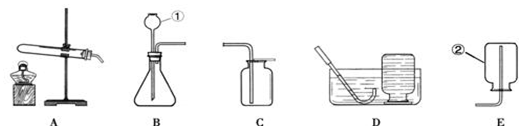
 如图是实 验室制取气体的常用装置.请回答:
如图是实 验室制取气体的常用装置.请回答: