题目内容
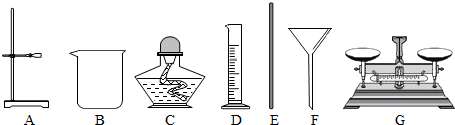
4.某化学兴趣小组利用下图装置探究制取气体的原理、方法.结合装置图,回答下列问题:
(1)写出图中标号仪器的名称:a分液漏斗,b锥形瓶;
(2)①过氧化氢溶液和二氧化锰制取氧气的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
②用过氧化氢溶液和二氧化锰制取氧气时,可选用的发生装置是B(填字母序号,下同),检查该发生装置气密性的方法是关闭分液漏斗活塞,把导管伸入水中,双手紧捂锥形瓶,如果导管口出现气泡,说明装置不漏气,可选用D装置收集氧气,其原因是氧气不易溶于水;
③下列是制取氧气的操作,正确的操作顺序是bacdfe;
a.将药品装入容器中,塞上带有导管的橡皮塞;b.检查装置气密性;c.收集氧气;d.检验氧气是否集满;e.拆除装置,将废弃物倒入指定容器内;f.将收集好的正放在桌上.
(3)用大理石和稀盐酸制取一瓶二氧化碳时,装置连接为BC.
(4)实验室常用氯化铵固体与碱石灰固体共热制取氨气(NH3),应选择的发生装置是A.
分析 (1)要熟悉各种仪器的名称、用途和使用方法;
(2)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
凡是有气体参加或产生的实验,实验前一定要检查装置的气密性,以防装置漏气影响实验结果;
氧气的密度比空气大,不易溶于水;
(3)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;
二氧化碳能够溶于水,密度比空气大;
(4)根据制取气体的反应物状态、反应条件、气体的性质可以选择发生装置和收集装置.
解答 解:(1)a是分液漏斗,通过分液漏斗可以向反应容器中注入液体药品;b是锥形瓶,常用作反应容器.
故填:分液漏斗;锥形瓶.
(2)①过氧化氢溶液和二氧化锰制取氧气的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
②用过氧化氢溶液和二氧化锰制取氧气时不需要加热,可选用的发生装置是B;
检查该发生装置气密性的方法是:关闭分液漏斗活塞,把导管伸入水中,双手紧捂锥形瓶,如果导管口出现气泡,说明装置不漏气;
可选用D装置收集氧气,其原因是氧气不易溶于水;
③下列是制取氧气的操作,正确的操作顺序是:检查装置气密性,将药品装入容器中,塞上带有导管的橡皮塞,收集氧气,检验氧气是否集满,将收集好的正放在桌上,拆除装置.
故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;B;关闭分液漏斗活塞,把导管伸入水中,双手紧捂锥形瓶,如果导管口出现气泡,说明装置不漏气;氧气不易溶于水;bacdfe.
(3)用大理石和稀盐酸制取一瓶二氧化碳时不需要加热,应该用B装置作为发生装置;
二氧化碳能够溶于水,不能用排水法收集,密度比空气大,可以用向上排空气法收集,即用C装置收集.
故填:BC.
(4)实验室用氯化铵固体与碱石灰固体制取氨气需要加热,应选择的发生装置是A.
故填:A.
点评 本题主要考查仪器的用途、反应表达式的书写,实验装置的选择,选择发生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气体的水溶性、能否和水发生化学反应、密度、能否和空气中的物质发生化学反应等因素.

 名校课堂系列答案
名校课堂系列答案| 选项 | 物质 | 杂质 | 除去杂质的方法 |
| A | O2 | CO2 | 通过碱石灰 |
| B | Cu粉 | Fe粉 | 加入过量稀盐酸,过滤 |
| C | CO2 | CO | 通入氧气点燃 |
| D | FeCl2溶液 | CuCl2 | 加过量Fe粉,过滤 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 石油分馏 | B. | 煤的气化 | ||
| C. | 工业上分离空气制得氧气 | D. | 干冰制冷 |
| A. | 金属镁着火不能用CO2灭火器灭火 | |
| B. | 镁在二氧化碳中燃烧的化学方程式为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C | |
| C. | 镁条在空气中燃烧时只与CO2发生了化学反应 | |
| D. | 不是一切物质的燃烧都要在空气或氧气中才能进行 |
| A. | 矿泉水瓶 | B. | 果皮 | C. | 旧报纸 | D. | 易拉罐瓶 |
| A. | -1 | B. | +1 | C. | +2 | D. | +4 |
 小昊用氢氧化钙、碳酸钠、氢氧化钠、盐酸和二氧化碳五种物质玩化学拼图游戏(如图),游戏规则要求图中相邻物质之间能发生反应.其中B是人体胃液中含有的酸,B与E反应无明显现象.
小昊用氢氧化钙、碳酸钠、氢氧化钠、盐酸和二氧化碳五种物质玩化学拼图游戏(如图),游戏规则要求图中相邻物质之间能发生反应.其中B是人体胃液中含有的酸,B与E反应无明显现象.