题目内容
20.某铁矿石的主要成分是Fe2O3,是冶炼金属铁的原料.某兴趣小组想测定该铁矿石中铁的含量,利用氢气来还原Fe2O3,设计了如下实验方案(铁矿石中的杂质在高温下不分解,也不参加反应).
(1)如果用锌粒与浓盐酸来制取氢气,可以选择图甲中的②(填序号)发生装置;装置②的主要仪器有分液漏斗、带导管的双孔胶塞和锥形瓶(填仪器名称).
(2)制得的氢气常含有少量水蒸气和HCl气体,若要得到干燥纯净的氢气,需通过④和⑤装置,装置按字母连接的顺序是:发生装置→c→d→b→a→收集装置

若要检验氢气中的杂质HCl,可把装置⑤(填序号)中的试剂换成紫色石蕊试液,实验中观察到的现象是试剂变成了红色.
(3)图甲中的③装置是一个用排空气法收集氢气的装置,由集气瓶和导管组成,请你在方框内画出该装置.
(4)图乙是氢气与铁矿石样品反应的装置,在加热反应之前要先通入一段时间的氢气,原因是排尽装置中的空气,防止H2不纯在加热时发生爆炸;而在反应结束时先要停止加热,一段时间后再停止通入氢气,原因是防止高温的铁在空气被氧化成氧化铁.
分析 依据反应物的状态和反应条件来确定发生装置,依据生成的气体的密度和水溶性来确定收集装置.
解答 解:(1)制取氢气用锌粒和盐酸反应.故发生装置选②,所用仪器为锥形瓶、分液漏斗、导管等.
(2)制取的氢气中因含有水蒸气和氯化氢气体,所以我们先除去氯化氢气体,再除去水蒸气.检验氢气中的杂质HCl时,我们用石蕊溶液来确定.所以我们可以把洗气瓶内的氢氧化钠换成石蕊试液.
(3)得分点:瓶口的方向;导管的长度,应为氢气的密度比空气小所以瓶口向下,导管深入到集气瓶底部是为了能把集气瓶内的空气更好的排净.
(4)凡是可燃性气体与氧气混合都有可能发生爆炸所以要在加热前赶走装置内的空气,防止余热的生成物铁重新被空气氧化,在加热的情况下铁会和空气中的氧气反应,故继续通氢气使其冷却.
答案:
(1)②分液漏斗;锥形瓶;
(2)c;d;b;a;⑤紫色石蕊试液;
(3)
(4)排尽装置中的空气,防止H2不纯在加热时发生爆炸;防止高温的铁在空气被氧化成氧化铁.
点评 此题考查知识点较多,既有氢气制取也有相关实验的操作要点,更有气体除杂及杂质气体的验证.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.超临界CO2流体是一种与水相似、能阻燃、溶解能力强的溶剂,被誉为“绿色环保溶剂”.在替代氟利昂作制冷剂方面也具有重要价值.下列说法错误的是( )
| A. | 超临界CO2与常态下CO2的物理性质不同,化学性质相同 | |
| B. | 超临界CO2能代替许多有害、有毒、易燃的有机溶剂 | |
| C. | 用超临界CO2替代氟利昂可以减轻对臭氧层的破坏 | |
| D. | 超临界CO2是一种特殊的物质,容易燃烧 |
8.下列除去物质中所含杂质的方法正确的是( )
| 物 质 | 杂 质 | 除杂试剂 | 提 纯 方 法 | |
| A | KCl | MnO2 | 水 | 充分溶解、过滤、蒸发 |
| B | CO2 | CO | O2 | 点燃 |
| C | NaCl | Na2CO3 | 硝酸 | 足量加入硝酸溶液 |
| D | AgNO3溶液 | Cu(NO3)2 | Cu粉 | 加入少量的铜粉,过滤 |
| A. | A | B. | B | C. | C | D. | D |
5.下列有关分子、原子和离子的说法正确的是( )
| A. | 分子是保持物质性质的一种粒子 | |
| B. | 原子转变成离子过程中电子数发生改变 | |
| C. | 物质的热胀冷缩现象主要是因为物质中的粒子大小随温度的改变而改变 | |
| D. | 在化学反应中,任何离子都不能再分 |
10.下列实验操作或装置正确的是( )
| A. | 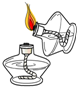 点燃酒精灯 | B. | 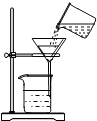 过滤 | ||
| C. | 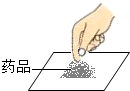 取粉末状固体药品 | D. | 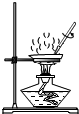 蒸发 |


 ”和“
”和“ ”表示两种不同的原子.
”表示两种不同的原子.