题目内容
某物质在氧气中完全燃烧,生成CO2和H2O的质量之比为22:9,则该物质的化学式可能是( )
| A、CO |
| B、CH3OH |
| C、C2H2 |
| D、C2H4 |
考点:有关化学式的计算和推断
专题:化学式的计算
分析:根据质量守恒定律分析,化学反应前后元素的种类和质量不变,生成物中碳元素和氢元素的质量比即为反应物中碳元素和氢元素的质量比.可燃物燃烧生成二氧化碳,说明可燃物中含碳元素;生成水,说明可燃物中含氢元素.
解答:解:根据质量守恒定律分析,化学反应前后元素的种类和质量不变,生成物中碳元素和氢元素的质量比即为反应物中碳元素和氢元素的质量比.可燃物燃烧生成二氧化碳,说明可燃物中含碳元素;生成水,说明可燃物中含氢元素.
生成物中碳元素和氢元素的质量比=(22×
):(9×
)=6:1,故碳原子和氢原子的个数比为:
:
=1:2,
通过观察,可知只有D中碳原子和氢原子的个数比为1:2
故选D.
生成物中碳元素和氢元素的质量比=(22×
| 12 |
| 44 |
| 2 |
| 18 |
| 6 |
| 12 |
| 1 |
| 1 |
通过观察,可知只有D中碳原子和氢原子的个数比为1:2
故选D.
点评:本道题总的来说属于有关化学方程式的计算,但解题关键还是有关化学式计算中的求物质中各元素的质量比.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
我市盛产茶叶,雨花茶享誉省内外.茶中的单宁酸具有抑制血压上升、清热解毒、抗癌等功效,其化学式为C76H52O46,下列说法不正确的是( )
| A、单宁酸由碳、氢、氧三种元素组成 |
| B、一个单宁酸分子由76个碳原子、52个氢原子和46个氧原子构成 |
| C、单宁酸分子中碳、氢、氧元素的质量比为228:13:184 |
| D、一个单宁酸分子中含26个氢分子 |
下列物质的用途主要由其物理性质决定的是( )
| A、用熟石灰改良酸性土壤 |
| B、铜用于制作导线 |
| C、糖类和油脂为人体活动提供能量 |
| D、用生石灰作干燥剂 |
下列反应中属于中和反应的是( )
| A、H2CO3═H2O+CO2↑ |
| B、Ba(OH)2+2HCl═BaCl2+2H2O |
| C、2KOH+CO2═K2CO3+H2O |
| D、CaO+2HCl═CaCl2+H2O |
食品安全与人体健康密切相关.下列做法不会损害人体健康的是( )
| A、吃变蛋(或松花蛋)时,为消除蛋中所含碱性物质的涩味,可加入少量食醋 |
| B、食用地沟油不会影响人体健康 |
| C、用甲醛的水溶液浸泡水产品 |
| D、用霉变花生制成的压榨花生油烹调食品 |
下列对碳和碳的氧化物的说法不正确的是( )
| A、C可以将CuO中的Cu置换出来 |
| B、在一定条件下CO能够转变成CO2 |
| C、CO2 能使被石蕊染成紫色的干花变红 |
| D、金刚石、石墨和C60都是碳元素的单质 |
下列离子在溶液中可以大量共存的一组是( )
| A、H+、Na+、OH- |
| B、Na+、NO3-、Cl- |
| C、H+、K+、HCO3- |
| D、Ca2+、SO42-、CO32- |
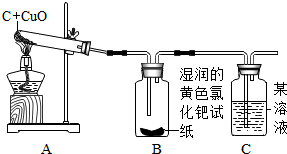 小兵和小东是某校化学研究性学习小组的成员,他们在查阅资料时,发现单质碳能够在高温时与金属氧化物反应得到金属单质.于是,他们用木炭与CuO进行了如下的探究活动.请你参与他们的这次活动,并解决的关问题:
小兵和小东是某校化学研究性学习小组的成员,他们在查阅资料时,发现单质碳能够在高温时与金属氧化物反应得到金属单质.于是,他们用木炭与CuO进行了如下的探究活动.请你参与他们的这次活动,并解决的关问题: