题目内容
向含有AgNO3、Cu(NO3)2和Mg(NO3)2的混合溶液中加入一定量的铁粉,待充分反应后过滤,向得到的滤渣中加入稀盐酸,发现有气体产生,请回答:
(1)滤渣中的物质有 ,滤液中的溶质 ;
(2)请写出铁粉与硝酸银溶液反应的化学方程式 .
(1)滤渣中的物质有
(2)请写出铁粉与硝酸银溶液反应的化学方程式
考点:金属的化学性质,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:据金属活动性顺序可知,镁>铁>铜>银,向含有AgNO3、Cu(NO3)2的混合溶液中加入一定量的铁粉,铁粉会首先置换硝酸银中的银,待硝酸银完全反应后继续与硝酸铜发生反应,铁与Mg(NO3)2不反应;过滤,向滤渣中滴加稀盐酸,有气泡产生,说明滤渣金属中含有铁,即加入的铁粉过量.
解答:解:因为向滤渣中滴加稀盐酸,有气泡产生,说明滤渣中有铁粉,即所加的铁粉过量,那说明原混合溶液中的银和铜全部被置换出来,即滤液中肯定没有AgNO3、Cu(NO3)2,则滤出的固体中一定含有Ag、Cu、Fe;因为铁和AgNO3、Cu(NO3)2反应时生成的是Fe(NO3)2,铁与Mg(NO3)2不反应;所以滤液中肯定有Mg(NO3)2、Fe(NO3)2;
所涉及的化学方程式分别为:Fe+2AgNO3=Fe(NO3)2+2Ag;Fe+Cu(NO3)2=Fe(NO3)2+Cu.
故答案为:
Ag、Cu、Fe;Mg(NO3)2、Fe(NO3)2;Fe+2AgNO3=Fe(NO3)2+2Ag.
所涉及的化学方程式分别为:Fe+2AgNO3=Fe(NO3)2+2Ag;Fe+Cu(NO3)2=Fe(NO3)2+Cu.
故答案为:
Ag、Cu、Fe;Mg(NO3)2、Fe(NO3)2;Fe+2AgNO3=Fe(NO3)2+2Ag.
点评:本题考查的是金属活动顺序表的应用,要能应用必须先把金属活动顺序表熟练的掌握住.此题考查的知识比较简单,属于基础题型.

练习册系列答案
 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
下列有关微粒结构的推理,结论正确的是( )
| A、原子中质子数等于电子数,离子是带电荷的原子,所以离子中质子数等于电子数 |
| B、元素的化学性质主要由最外层电子数决定,镁原子和氦原子最外层均2个电子,所以化学性质相似 |
| C、化学变化产生了新物质,故在化学变化中,原子和分子都会变化 |
| D、元素的种类由质子数决定,钠原子和氯原子中质子数分别为11和17,所以属于不同元素 |

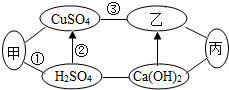 如图中甲、乙、丙是初中化学常见的三种物质,它们属于不同类型.图中“-”表示 相连的物质之间可以在溶液中发生化学反应,“→”表示由某种物质可以转化为另一种物质.(部分反应物,生成物已略去)
如图中甲、乙、丙是初中化学常见的三种物质,它们属于不同类型.图中“-”表示 相连的物质之间可以在溶液中发生化学反应,“→”表示由某种物质可以转化为另一种物质.(部分反应物,生成物已略去)