题目内容
某化工厂为了综合利用生产过程中的副产品CaSO4,与相邻的化肥厂联合设计了以下制备(NH4)2SO4的工艺流程.在下图流程中,沉淀池里物质发生的主要化学反应为:CO2+2NH3+CaSO4+H2O=CaCO3↓+(NH4)2SO4.
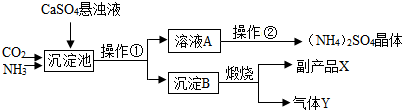
(1)沉淀B高温煅烧反应的化学方程式 ,反应的基本类型: ,该工艺中可循环使用的物质为 (填化学式).
(2)实验室里操作①称为 ,实验室进行此操作时,用到的玻璃仪器有玻璃棒、 、 .操作②的过程是加热浓缩、 、结晶,获得(NH4)2SO4晶体.
(3)从绿色化学和资源综合利用的角度说明上述流程的主要优点是 .

(1)沉淀B高温煅烧反应的化学方程式
(2)实验室里操作①称为
(3)从绿色化学和资源综合利用的角度说明上述流程的主要优点是
考点:物质的相互转化和制备,过滤的原理、方法及其应用,盐的化学性质,反应类型的判定,书写化学方程式、文字表达式、电离方程式
专题:物质的制备
分析:(1)沉淀B为碳酸钙,碳酸钙高温煅烧生成氧化钙和二氧化碳;根据化学方程式判断反应类型;
(2)使沉淀与溶液分离的方法是过滤,硫酸铵由溶液中结晶析出的方法是冷却热饱和溶液的方法;
(3)这一实验的主要优点是不污染环境,有些原料可循环使用.
(2)使沉淀与溶液分离的方法是过滤,硫酸铵由溶液中结晶析出的方法是冷却热饱和溶液的方法;
(3)这一实验的主要优点是不污染环境,有些原料可循环使用.
解答:解:
(1)沉淀B为碳酸钙,碳酸钙高温煅烧生成氧化钙和二氧化碳;有一种反应物生成两种或两种以上其他物质的反应叫做分解反应;在前面的反应中是反应物,后面的反应中是生成物,这样的物质可循环使用,由流程可知CO2是该工艺中可循环使用的物质;
(2)使碳酸钙与溶液分离的方法是过滤,实验室进行此操作时,用到的玻璃仪器有玻璃棒、烧杯、漏斗.使硫酸铵从溶液中结晶析出的方法是先加热制成饱和溶液,再降温冷却,结晶析出;
(3)这一实验的主要优点是不污染环境,有些原料可循环使用.
故答案为:
(1)CaCO3
CaO+CO2↑;分解反应;CO2;
(2)过滤;烧杯、漏斗;冷却;
(3)产生的CO2循环使用;得到的产品和副产品都是有用的物质,无废物产生.
(1)沉淀B为碳酸钙,碳酸钙高温煅烧生成氧化钙和二氧化碳;有一种反应物生成两种或两种以上其他物质的反应叫做分解反应;在前面的反应中是反应物,后面的反应中是生成物,这样的物质可循环使用,由流程可知CO2是该工艺中可循环使用的物质;
(2)使碳酸钙与溶液分离的方法是过滤,实验室进行此操作时,用到的玻璃仪器有玻璃棒、烧杯、漏斗.使硫酸铵从溶液中结晶析出的方法是先加热制成饱和溶液,再降温冷却,结晶析出;
(3)这一实验的主要优点是不污染环境,有些原料可循环使用.
故答案为:
(1)CaCO3
| ||
(2)过滤;烧杯、漏斗;冷却;
(3)产生的CO2循环使用;得到的产品和副产品都是有用的物质,无废物产生.
点评:做推断题时要充分利用所给的信息,结合自己已学过的知识,进行有依据性的推测.

练习册系列答案
相关题目
下列图示的实验操作正确的是( )
A、 过滤 |
B、 称取氯化钠 |
C、 稀释浓硫酸 |
D、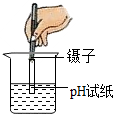 测溶液的PH值 |
下列做法不会改变PM2.5检测结果的是( )
| A、海水晒盐 |
| B、燃放鞭炮 |
| C、露天焚烧垃圾 |
| D、工厂排放烟尘 |
下列叙述中属于化学变化的是( )
| A、电灯通电发光 | B、石油分馏 |
| C、食物腐烂 | D、酒精挥发 |