题目内容
19.某课外活动小组的同学将16克氧化铜和过量的炭粉均匀混合,用如图1所示装置进行实验.图中铁架台等装置已略去.请回答有关问题:(1)实验中最多能得到铜12.8克.
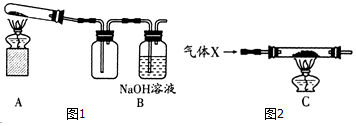
(2)同学们想通过测定消耗碳、氧元素的质量和生成二氧化碳的质量,以进一步分析氧化铜和炭粉反应产生的气体除CO2外是否还有其它产物.反应一段时间后停止加热,冷却到室温.反应前.后测得的数据如下:
| 装置 | 反应前 | 反应后 |
| A | 试管的质量36.2 克 氧化铜和炭粉混合物的质量20.0克 | 试管和固体物质的质量54.8 克 |
| B | 反应后瓶内液体比反应前增重1.1 克 | |
A.装置中还有一部分CO2未被NaOH溶液吸收
B.氧化铜和炭粉反应产生的气体除CO2外还有CO
C.氧化铜和炭粉没有完全反应
D.该反应不符合质量守恒定律
(3)有同学认为用图2所示装置C代替上面的装置A,加热前先通一会气体X,停止加热后再通一会该气体,这样可使实验测得的数据更能准确的说明问题.你认为在O2、N2和H2三种气体中,X应选择哪一种气体?
N2.
分析 (1)根据氧化铜的质量和化学方程式计算出铜的质量;
(2)根据质量守恒定律求出反应前后的质量差和1.1g比较进行分析.
可从反应条件及装置中气体是否被充分吸收角度进行分析;
(3)根据X是否参与反应影响实验及安全性角度分析.
解答 解:(1)设实验中最多能得到铜的质量为x.
根据2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑
160 128
16g x
列比例式为$\frac{160}{128}=\frac{16g}{x}$,解得x=12.8g,所以铜的质量为12.8克.故答案为:12.8;
(2)根据质量守恒定律知反应前后的质量差即为反应的碳和氧的质量,为56.8g-38.2g-20.0g=1.4g>1.1g,说明反应中消耗碳和氧元素的质量大于生成二氧化碳的质量.主要原因是由于装置的滞留的二氧化碳不能被吸收,同时反应时还可能发生反应C+CuO$\frac{\underline{\;高温\;}}{\;}$Cu+CO↑,部分碳没有转换为二氧化碳.故填:大于;AB.
(3)因为氧气要和碳发生反应,反应结束后要和生成的铜反应,影响实验结果;
氢气具有可燃性,且不安全使用时必须验纯,所以选氮气,故填:N2.
故答案为:
(1)12.8;(2)大于;AB.(3)N2.
点评 ①熟练掌握实验技能,②灵活运用质量守恒定律,根据化学方程式的计算③掌握碳的化学性质.

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案
相关题目
10.下列所示的生物中,含水量最多的是( )
| A. | 人 | B. | 海藻 | C. | 水母 | D. | 鹦鹉 |
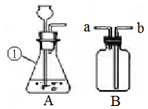 通过近一年的化学学习,你已经掌握了实验室制取气体的有关方法.请根据下图回答问题:
通过近一年的化学学习,你已经掌握了实验室制取气体的有关方法.请根据下图回答问题: