题目内容
19.实验室部分仪器或装置如图所示,请回答下列问题:
(1)实验室用高锰酸钾制取氧气文字表达式为高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气.
(2)上述装置中,可用于加热高锰酸钾制取氧气的气体发生装置的是A(填仪器装置下方的字母,下同),收集装置可选用图中的C或E,收集方法的依据分别是氧气密度比空气大或氧气不易溶于水.检验氧气是否收集满的方法是将带火星的木条伸到集气瓶口,木条复燃证明氧气已集满.
分析 (1)高锰酸钾分解产生氧气、二氧化锰和锰酸钾据此书写反应表达式;
(2)高锰酸钾制氧气是固体药品在加热条件下反应,据此选择发生装置,根据氧气的密度和溶解性选择其收集方法,根据氧气有助燃性选择验满方法.
解答 解:(1)高锰酸钾加热生成锰酸钾、二氧化锰和氧气,反应的文字表达式为:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;
(2)高锰酸钾制氧气需要加热故选择A装置做为发生装置;氧气密度比空气大,故选择C装置来收集氧气;氧气不易溶于水,故选择E装置来收集氧气,氧气能使带火星的木条复燃,验满时将带火星的木条伸入到集气瓶口,木条复燃证明氧气已集满.
答案:(1)高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;
(2)A;C;E;氧气密度比空气大;氧气不易溶于水;将带火星的木条伸到集气瓶口,木条复燃证明氧气已集满.
点评 本考点主要考查了气体的制取装置和收集装置的选择,气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
相关题目
9.染发时常用到的着色剂--对苯二胺,是一种有毒的化学药品,有致癌性,会对染发者的身体带来伤害,其化学式为C6H8N2.有关对苯二胺的说法正确的是( )
| A. | 对苯二胺属于化合物 | |
| B. | 对苯二胺的相对分子质量为27 | |
| C. | 对苯二胺中碳、氢、氮元素的质量比为3:4:1 | |
| D. | 对苯二胺中碳.氢.氮原子个数比为18:2:7 |
10.区分某地下水(硬水)和蒸馏水,可以选用的物质是肥皂水;“岩盐之都”河南叶县盛产食盐.食盐的主要成分NaCl由离子(填“分子”、“原子”或“离子”)构成;除去食盐水中泥沙等不溶性杂质的方法是过滤.
11.下列物质属于单质的是( )
| A. | 水 | B. | 水银 | C. | 氧化铜 | D. | 矿泉水 |
12.下列化学方程式书写正确的是( )
| A. | CO+O2═CO2 | B. | CO2+Ca(OH)2═CaCO3+H2O | ||
| C. | 2KMnO4═K2MnO4+MnO2+O2 | D. | CuSO4+2NaOH═Na2SO4+Cu(OH)2↓ |
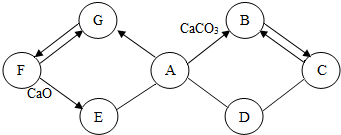 如图所示A~G是初中化学常见的物质.图中“→”表示转化关系,“-”表示相互能反应.已知A是人体胃液中含有的酸,G是气体单质,B和C含有相同的元素.
如图所示A~G是初中化学常见的物质.图中“→”表示转化关系,“-”表示相互能反应.已知A是人体胃液中含有的酸,G是气体单质,B和C含有相同的元素.
 按如图组装仪器,关闭止水夹,通电后使红磷燃烧.请回答下列问题:
按如图组装仪器,关闭止水夹,通电后使红磷燃烧.请回答下列问题: