题目内容
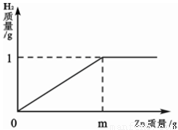
已知烧杯中装有200g硫酸和硫酸锌混合溶液,其中含硫酸锌12.1g.向烧杯中逐渐加入锌粒,放出气体质量与加入锌粒质量的关系如图所示.当恰好完全反应时,所得的溶液为不饱和溶液.请计算:
(1)m=_________(2)原混合溶液中H2SO4的质量分数为_________.
(1) 32.5??? (2)24.5%
【解析】
试题分析:(1)据右上图可知,最终生成的氢气质量是1g,根据发生的化学反应方程式:H2SO4 +Zn?????? =ZnSO4 + H2↑中锌与氢气的质量关系,即可算出消耗的锌的质量,同理,根据H2SO4和氢气的质量关系,也可算出硫酸的质量,再利用质量分数的表达式即可求解:
解:设参加反应锌的质量为m,消耗H2SO4的质量为x
H2SO4 +Zn = ZnSO4 + H2↑
98??? 65?????????? 2
X???? m??????????? 1g
65:2=m:1g???? ∴m=32.5g
98:2=x:1g???? ∴x=49g?????? 原混合溶液中H2SO4的质量分数为=49g/200g×100%=24.5%
考点:根据化学方程式进行计算

 走进文言文系列答案
走进文言文系列答案| 加入NaOH溶液的质量/g | 50.0 | 100.0 | 150.0 | 200.0 | 250.0 |
| 生成沉淀的质量/g | 0.0 | 2.5 | 8.6 | 9.8 | 9.8 |
(2)参加反应的NaOH溶液的总质量是多少克?(要求写出计算过程)
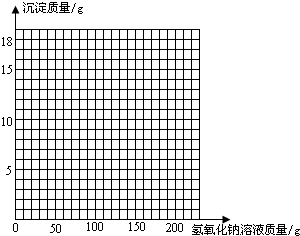
(3)画出在该混合溶液中加入NaOH溶液质量与生成沉淀质量变化关系的曲线(见答题卡).
| 加入NaOH溶液的质量/g | 50.0 | 100.0 | 150.0 | 200.0 | 250.0 |
| 生成沉淀的质量/g | 0.0 | 2.45 | 8.6 | 9.8 | 9.8 |
(2)参加反应的NaOH溶液的总质量是多少克?(要求写出计算过程)
烧杯中装有一定量硫酸和硫酸铜的混合溶液,已知该溶液中含H2SO4的质量为9.8g。某同学为测定该混合溶液中硫酸铜的质量,向烧杯中逐渐加入10%的NaOH溶液,得到沉淀的质量记录如下:
| 加入NaOH溶液的质量/g | 50.0 | 100.0 | 150.0 | 200.0 | 250.0 |
| 生成沉淀的质量/g | 0.0 | 2.5 | 8.6 | 9.8 | 9.8 |
(1)得到沉淀的总质量为 g,该混合溶液中硫酸铜的质量为 g。
(2)参加反应的NaOH溶液的总质量是多少克?(要求写出计算过程)
(3)画出在该混合溶液中加入NaOH溶液质量与生成沉淀质量变化关系的曲线(见答题卡)。
烧杯中装有一定量硫酸和硫酸铜的混合溶液,已知该溶液中含H2SO4的质量为9.8g。某同学为测定该混合溶液中硫酸铜的质量,向烧杯中逐渐加入10%的NaOH溶液,得到沉淀的质量记录如下:
| 加入NaOH溶液的质量/g | 50.0 | 100.0 | 150.0 | 200.0 | 250.0 |
| 生成沉淀的质量/g | 0.0 | 2.5 | 8.6 | 9.8 | 9.8 |
(1)得到沉淀的总质量为 g,该混合溶液中硫酸铜的质量为 g。
(2)参加反应的NaOH溶液的总质量是多少克?(要求写出计算过程)