题目内容
15. 如图是NaCl、MgSO4的溶解度曲线.下列说法正确的是( )
如图是NaCl、MgSO4的溶解度曲线.下列说法正确的是( )| A. | 只有在t1℃时,NaCl和MgSO4的溶解度才相等 | |
| B. | t2℃~t3℃,MgSO4的溶解度随温度升高而增大 | |
| C. | MgSO4的饱和溶液在t1℃时,溶质质量分数最大 | |
| D. | t2℃时的MgSO4饱和溶液降温至t1℃时,有晶体析出 |
分析 A、溶解度曲线的交点表示该温度下二者的溶解度相等;
B、据溶解度曲线可知物质的溶解度随温度变化情况;
C、饱和溶液中溶质的质量分数=$\frac{溶解度}{溶解度+100g}$×100%,可知溶解度大则溶质的质量分数大;
D、t1℃至t2℃,硫酸镁的溶解度逐渐增大,所以在此温度范围内降低其饱和溶液会析出晶体.
解答 解:A、由图可知:氯化钠和硫酸镁的溶解度曲线有两个交点,说明其溶解度相同时有两个温度,故错误;
B、t2℃~t3℃,MgSO4的溶解度随温度升高而减小,故错误;
C、饱和溶液中溶质的质量分数=$\frac{溶解度}{溶解度+100g}$×100%,可知溶解度大则溶质的质量分数大;MgSO4的溶解度在t2℃最大,所以饱和溶液在t2℃时,溶质质量分数最大,故错误;
D、t2℃至t1℃,硫酸镁的溶解度逐渐减小,所以t1℃时的MgSO4饱和溶液降温至t2℃时,有晶体析出,正确;
故选:D.
点评 明确溶解度概念、溶解度曲线的意义等知识,是解答问题的关键,能较好考查学生对知识的掌握和运用情况.

练习册系列答案
相关题目
4.研究金属的腐蚀对资源的利用和保护意义重大.
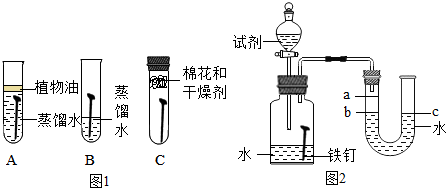
(1)为了探究铁锈蚀的条件,进行如图所示实验.经过一周后观察,试管A和C中的铁钉无明显变化,试管B中的铁钉明显锈蚀.
①通过实验发现:铁锈蚀是铁与氧气和水发生化学反应的过程.
②A中加入的蒸馏水要事先煮沸,其目的是除去水中的氧气.
(2)家中的刀具若沾有食盐水锈蚀更快.为了进一步探究影响铁锈蚀速率的因素,做了如下的实验.
【提出问题】铁锈蚀速率与哪些因素有关.
【查阅资料】①物质溶解在水中得到的混合物称为水溶液,如氯化钠溶解在水中得到氯化钠溶液,乙醇溶解在水中得到乙醇溶液.
②氯化钠溶液能导电;乙醇溶液不能导电.
【猜想】铁的锈蚀速率与下列因素有关:
①反应时的温度;②水溶液的导电性.
【实验】每次取两套如图所示的装置,编号为I、II.向两套装置中分别装入质量、大小相同的铁钉和等体积的蒸馏水,进行如下三组对比实验(实验开始时,各瓶内气体压强保持一致).
(1)为了探究铁锈蚀的条件,进行如图所示实验.经过一周后观察,试管A和C中的铁钉无明显变化,试管B中的铁钉明显锈蚀.

①通过实验发现:铁锈蚀是铁与氧气和水发生化学反应的过程.
②A中加入的蒸馏水要事先煮沸,其目的是除去水中的氧气.
(2)家中的刀具若沾有食盐水锈蚀更快.为了进一步探究影响铁锈蚀速率的因素,做了如下的实验.
【提出问题】铁锈蚀速率与哪些因素有关.
【查阅资料】①物质溶解在水中得到的混合物称为水溶液,如氯化钠溶解在水中得到氯化钠溶液,乙醇溶解在水中得到乙醇溶液.
②氯化钠溶液能导电;乙醇溶液不能导电.
【猜想】铁的锈蚀速率与下列因素有关:
①反应时的温度;②水溶液的导电性.
【实验】每次取两套如图所示的装置,编号为I、II.向两套装置中分别装入质量、大小相同的铁钉和等体积的蒸馏水,进行如下三组对比实验(实验开始时,各瓶内气体压强保持一致).
| 影响因素 | 实验设计实验 | 现象 | 实验结论 |
| ①温度 | 装置I放入25℃恒温环境中,装置II放入40℃恒温环境中. | 两套装置中铁钉均锈蚀,且U型管中液面均由b处上升至a处,则所需时间I>II. | 铁的锈蚀速率与反应时的温度有关, 温度越高,铁的锈蚀速率越快 |
| ②水溶液的导电性 | 在相同温度下,装置I集气瓶中加入10mL氯化钠溶液;装置II集气瓶中加入10mL乙醇. | 两套装置中铁钉均锈蚀;且U型管中液面均由b处上升至a处,则所需时间I<II. | 铁的锈蚀速率与水溶液的导电性有关,在能导电的溶液中,锈蚀的速率加快 |
5.物质的性质决定其保存方法.氢氧化钠固体必须密封保存的主要原因是( )
| A. | 白色固体 | B. | 有腐蚀性 | ||
| C. | 易吸收水分 | D. | 能与空气中的二氧化碳反应 |
 ;
;