题目内容
10.如图是实验室制取气体的一些装置,据图回答问题.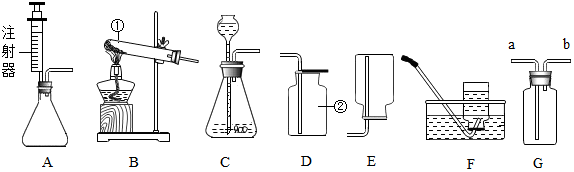
(1)若实验室要用C装置作氧气的发生装置,所用的药品是双氧水和二氧化锰;用F装置收集氧气,需等到导管口有连续均匀气泡冒出时才能开始收集.
(2)若实验室要用高锰酸钾为原料用装置B制氧气,试管口还要放一团棉花,该反应的符号表达式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)若用D装置收集氧气,验满的方法是:将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了
(4)老师提出用碳酸钠粉末与稀盐酸制取二氧化碳.常温下,碳酸钠(Na2CO3)与稀盐酸(HCl)反应生成氯化钠、水和二氧化碳,其反应的符号表达式为Na2CO3+2HCl=2NaCl+H2O+CO2↑,但该反应的速率非常快,为了较好地完成该实验,你认为图中最适合制取二氧化碳气体的发生装置是A(填装置序号);已知二氧化碳的密度比空气大,如果用装置G收集二氧化碳,气体应从a(填“a”或“b”)端管口通人.
分析 制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.用排水法收集较纯净氧气的适宜时间是:当导管口有连续均匀气泡冒出时;氧气的验满方法是:将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了;碳酸钠和盐酸反应生成氯化钠和水和二氧化碳,配平即可;注射器可以控制反应的速率,已知二氧化碳的密度比空气大,如果用装置G收集二氧化碳,气体应从长管进入.
解答 解:(1)如果用双氧水和二氧化锰制氧气就不需要加热,用排水法收集较纯净氧气的适宜时间是:当导管口有连续均匀气泡冒出时;故答案为:双氧水和二氧化锰;导管口有连续均匀气泡冒出时;
(2)加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;故答案为:一团棉花;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)氧气的验满方法是:将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了;故答案为:将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了;
(4)碳酸钠和盐酸反应生成氯化钠和水和二氧化碳,配平即可;注射器可以控制反应的速率,已知二氧化碳的密度比空气大,如果用装置G收集二氧化碳,气体应从长管进入;故答案为:Na2CO3+2HCl=2NaCl+H2O+CO2↑;A;a;
点评 本考点主要考查了药品的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和气体的验满等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案| A. | 两个氮分子:2N | B. | 镁离子:Mg+2 | C. | 两个氢原子:2H2 | D. | 氧化镁:MgO |
(1)HClO在常温下分解,反应为2HClO=2HCl+O2↑.某瓶HClO溶液放置一段时间后,溶液的pH减小 (填“增大”或“减小”或“不变”).
(2)在漂白粉中滴加盐酸,能加快漂白的速率.写出漂白粉中加入盐酸反应的化学方程式Ca(ClO)2+2HCl=CaCl2+2HClO.
(3)有一包长时间放置的漂白粉,想知道该漂白粉是否变质,某同学设计了下列探究实验.
【提出问题】长时间放置的漂白粉是否变质?
【猜 想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为CaCl2、Ca(ClO)2、CaCO3;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3.
【实验探究】限选试剂及仪器,盐酸、石灰水、品红溶液、试管、带导管的单孔塞.
| 实验操作与实验现象 | 实验结论 |
| ①取少量样品于试管中,加足量稀盐酸,观察到产生气泡. ②在上述反应后试管中加少量品红溶液.观察到品红溶液褪色. | 猜想2成立 |

【实验数据】实验共记录了两组数据:第①组,气体吸收完全后,NaOH溶液质量增加4.4g;第②组,沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为10g.根据实验设计及有关数据进行分析与计算:
混合溶液中HCl的质量分数为7.3%.(只写结果)
混合溶液中CaCl2的质量分数为多少?(写出计算过程)
| A. |  点燃酒精灯 点燃酒精灯 | B. |  | C. |  液体加热 液体加热 | D. |  |
(1)请你设计另一个不同的实验确认该氢氧化钠溶液已变质.
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量该溶液于试管中,滴加适量的氯化钙溶液 | 产生白色沉淀 | 该氢氧化钠溶 液已变质 |
| 实验步骤 | 实验现象 | 实验结论 |
取少量该溶液于试管中,滴加过量的氯化钙溶液; 静置一会儿后滴加酚酞试液 | 产生白色沉淀; 酚酞试液变红色 | 该氢氧化钠 溶液部分变质 |
反应的化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
| A. |  | B. |  | C. |  | D. |  |