题目内容
1.金属锂(元素符号为Li)在通讯和航空航天领域中具有极其重要的用途.它的化合物氢氧化锂[LiOH]是一种易溶于水的白色固体,有辣味,具有强碱性和腐蚀性.(1)“辣味”属于氢氧化锂的(填“物理”或“化学”,下同)物理性质;
“腐蚀性”属于氢氧化锂的化学性质.
(2)LiOH中锂元素的化合价为+1.
(3)载人航天飞船中通常用LiOH代替NaOH来吸收航天员呼吸产生的CO2,则LiOH与CO2反应的化学方程式2LiOH+CO2═Li2CO3+H2O.
(4)右表是部分物质的溶解性表,运用此溶解性表并结合你对复分解反应发生条件的理解,从表中选出一种盐,该盐能和LiOH发生复分解反应,请你写出该盐的化学式CuSO4或Cu(NO3)2.
| OH- | CO32- | SO42- | NO3- | |
| Ba2+ | 溶 | 不 | 不 | 溶 |
| Cu2+ | 不 | 不 | 溶 | 溶 |
| Li+ | 溶 | 微溶 | 溶 | 溶 |
分析 (1)物质的化学性质是指在化学变化中表现出来的性质,物质的物理性质是指不需要通过化学变化表现出来的性质;
(2)在化合物中,元素化合价的代数和为零;
(3)氢氧化锂和二氧化碳反应能生成碳酸锂和水;
(4)酸碱盐之间要发生复分解反应需符合复分解反应的条件,即有沉淀、气体或水生成.
解答 解:(1)氢氧化锂的“辣味”不需要通过化学变化表现出来,属于物理性质.故填:物理.
氢氧化锂的“腐蚀性”需要通过化学变化表现出来,属于化学性质.故填:化学.
(2)氢氧化锂中,氢氧根的化合价是-1,可以求出锂元素的化合价是+1.故填:+1.
(3)氢氧化锂和二氧化碳反应的化学方程式为:2LiOH+CO2═Li2CO3+H2O;故填:2LiOH+CO2═Li2CO3+H2O;
(4)LiOH溶液与表中离子组成的 一种盐的溶液反应,此盐与LiOH接触需要生成沉淀,此盐可为CuSO4或Cu(NO3)2,LiOH与CuSO4反应能生成Cu(OH)2沉淀和Li2SO4;LiOH与Cu(NO3)2反应能生成Cu(OH)2沉淀和LiNO3;
故答案为:CuSO4或Cu(NO3)2.
点评 本题考查了复分解反应的条件以及物质间的反应,完成此题,可以依据已有的知识结合表格内容进行.了解化学性质与物理性质的差别及其应用.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
11.兴趣小组同学发现,维C泡腾片的主要成分有维生素C(C6H9O6)、碳酸氢钠(NaHCO3)、柠檬酸(C6H8O7).维C泡腾片溶于水有许多气泡产生,小组同学对该气体的成分进行了如下探究:
【猜想与假设】
小明说:该气体可能是O2、H2、SO2、CO、CO2
小洋说:不可能含有SO2,因为根据质量守恒定律(或化学反应前后元素种类不变),反应物中不含硫元素.
小美说:不可能含有H2和CO,从药品安全角度考虑,H2易燃易爆,CO有毒,讨论后,小组同学认为该气体可能含O2、CO2中的一种或两种.
【进行实验】
【得出结论】由实验①可知,该气体中肯定含有二氧化碳;由实验②不能确定该气体中不含氧气,理由是若生成氧气和二氧化碳的混合物,当氧气含量过少时,带火星的木条也不能复燃.
【猜想与假设】
小明说:该气体可能是O2、H2、SO2、CO、CO2
小洋说:不可能含有SO2,因为根据质量守恒定律(或化学反应前后元素种类不变),反应物中不含硫元素.
小美说:不可能含有H2和CO,从药品安全角度考虑,H2易燃易爆,CO有毒,讨论后,小组同学认为该气体可能含O2、CO2中的一种或两种.
【进行实验】
| 实验编号 | 实验操作 | 实验现象 |
| ① | 将气体通入澄清的石灰水中 | 澄清石灰水变浑浊 |
| ② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
12.地质学家在浙江西北部发现了稀土矿.其中含有一种元素钪,钪呈银白色,质软,易溶于酸.一般在空气中迅速氧化而失去光泽.主要存在于极稀少的钪钇石中.可用于制特种玻璃及轻质耐高温合金等.以下关于钪的说法中错误的是( )
| A. | 钪是一种金属元素,产量较少 | B. | 钪的化学性质不活泼 | ||
| C. | 银白色和质软是钪的物理性质 | D. | 稀土矿是一种混合物 |
11.在化学王国里,数字被赋予了丰富的内涵,对下列化学用语中数字“2”的说法正确的是( )
①2H ②2NH3 ③SO2 ④Mg2+ ⑤2OH- ⑥H2O.
①2H ②2NH3 ③SO2 ④Mg2+ ⑤2OH- ⑥H2O.
| A. | 表示离子的个数的是④⑤ | B. | 表示离子所带电荷数的是④⑤ | ||
| C. | 表示分子个数的是①② | D. | 表示分子中原子个数的是③⑥ |
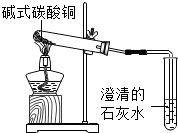 铜器长期暴露在空气中会生成铜绿(俗称铜锈).铜锈的主要成分是碱式碳酸铜,碱式碳酸铜不稳定,受热分解成黑色固体物质、无色气体和水.这种黑色固体和无色液体的成分是什么呢?
铜器长期暴露在空气中会生成铜绿(俗称铜锈).铜锈的主要成分是碱式碳酸铜,碱式碳酸铜不稳定,受热分解成黑色固体物质、无色气体和水.这种黑色固体和无色液体的成分是什么呢?