题目内容
19.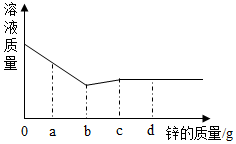 向一定量硝酸银、硝酸镁和硝酸铜的混合溶液中加入一定量的锌,溶液的质量与加入锌的质量的变化关系如图所示.请回答下列问题
向一定量硝酸银、硝酸镁和硝酸铜的混合溶液中加入一定量的锌,溶液的质量与加入锌的质量的变化关系如图所示.请回答下列问题(1)当加入锌的质量为ag时,溶液中有4种溶质.
(2)当加入锌的质量为dg时,溶液中的金属离子有镁离子、锌离子.
(3)请解释当加入锌的质量在b-cg时,溶液的质量增加的原因.
分析 根据四种金属的活动性顺序是:镁、锌、铜、银,所以向一定量的硝酸银、硝酸铜和硝酸镁的混合溶液中加入Zn,锌会先与硝酸银反应,然后再与硝酸铜反应,a→b溶液质量减小,发生的反应是锌和硝酸银反应生成硝酸锌和银,溶液质量逐渐减小,b→c段发生的反应是锌和硝酸铜反应生成硝酸锌和铜进行分析.
解答 解:四种金属的活动性顺序是:镁、锌、铜、银,所以向一定量的硝酸银、硝酸铜和硝酸镁的混合溶液中加入Zn,锌会先与硝酸银反应,然后再与硝酸铜反应,a→b溶液质量减小,发生的反应是锌和硝酸银反应生成硝酸锌和银,溶液质量逐渐减小,b→c段发生的反应是锌和硝酸铜反应生成硝酸锌和铜,所以
(1)当加入锌的质量为ag时,溶液质量没有减小到最小,说明硝酸银没有完全反应,溶液中有硝酸镁、硝酸铜、没有反应完的硝酸银、生成的硝酸锌4种溶质;
(2)当加入锌的质量为dg时,加入的锌是过量的,硝酸银、硝酸铜完全反应,溶液中的金属离子有镁离子、锌离子;
(3)当加入锌的质量在b-cg时,每65份质量的锌和硫酸铜反应生成硫酸锌和64份质量的铜,所以反应后溶液质量增加.
故答案为:(1)4;
(2)镁离子、锌离子;
(3)每65份质量的锌和硫酸铜反应生成硫酸锌和64份质量的铜,所以反应后溶液质量增加.
点评 活动性强的金属放入活动性弱的金属的混合盐溶液中,活动性强的金属会先把活动性最弱的金属从其盐溶液中置换出来,然后再置换活动性较弱的金属.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.吃火锅时,我们虽然没往锅内继续放盐,但汤越吃越咸,这是因为( )
| A. | 汤的上部淡下部咸 | |
| B. | 汤内锅底的盐没溶解 | |
| C. | 汤内盐的质量分数随着水份的蒸发而增大 | |
| D. | 其它原因 |
10.下列实验现象描述正确的是( )
| A. | 硫在氧气中燃烧火焰呈淡蓝色 | B. | 碳在空气中燃烧生成二氧化碳 | ||
| C. | 磷在空气中燃烧产生大量白色烟雾 | D. | 铁丝在氧气中剧烈燃烧,火星四射 |
7.下列化学方程式符合题意且书写正确的是( )
| A. | 用盐酸除铁锈:FeO+2HCl═FeCl2+H2O | |
| B. | 正常雨水的pH约为5.6的原因:CO2+H2O═H2CO3 | |
| C. | 除去CO2中少量的CO:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 | |
| D. | 除去氯化钙溶液中盐酸:CaO+2HCl═CaCl2+H2O |
14.开封灌汤包被誉为“中州膳食一绝”.制作包子的原料有:瘦肉、面粉、麻油、葱花和食盐等,灌汤包中富含的营养素有糖类(写出一种即可).食盐的主要成分NaCl由离子(填“分子”“原子”或“离子”)构成.
4.2010年“世界水日”的主题是“跨界水--共享的水、共享的机遇”.下列涉及水的变化中没有化学变化的是( )
| A. | 海水晒盐 | B. | 太阳能光解水制氢气 | ||
| C. | 饮用水生产时用ClO2消毒 | D. | 水作为原料参与植物光合作用 |
11.铁制品在通常情况下很易生锈,制造时往往在铁制品表面电镀一层铜起防锈作用.下列说法正确的是( )
| A. | 镀铜铁制品不易生锈的原因之一是使铁隔绝了空气 | |
| B. | 镀铜铁制容器可盛硝酸银溶液 | |
| C. | 镀铜铁制品不可以在弱酸性条件下使用 | |
| D. | 镀铜铁制品是一种合金 |
8.2010年冬奥会兴奋剂检测是对运动员的一项重要检验.其中一种兴奋剂的化学式为C20H26O2,下列关于该兴奋剂的说法正确的是( )
| A. | 将该兴奋剂在足量的氧气中充分燃烧,产物为CO2和H2O | |
| B. | 该兴奋剂是由多原子构成的无机化合物 | |
| C. | 该兴奋剂是由20个碳原子、26个氢原子和2个氧原子构成 | |
| D. | 该兴奋剂中碳、氢、氧三种元素的质量比为20:26:2 |
9.下列有关有机合成材料的叙述,错误的是( )
| A. | 有机合成材料的主要成分是高分子化合物 | |
| B. | 有机合成材料通常有合成塑料.合成纤维和合成橡胶 | |
| C. | 有机合成材料通常是易燃物 | |
| D. | 有机合成材料的可塑性都很大 |