题目内容
7.下列化学方程式符合题意且书写正确的是( )| A. | 用盐酸除铁锈:FeO+2HCl═FeCl2+H2O | |
| B. | 正常雨水的pH约为5.6的原因:CO2+H2O═H2CO3 | |
| C. | 除去CO2中少量的CO:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 | |
| D. | 除去氯化钙溶液中盐酸:CaO+2HCl═CaCl2+H2O |
分析 根据方程式的正误判断方法:先看反应是否能进行,再看化学式是否书写正确,再看是否配平,再看条件,最后看是否改成了等号.
解答 解:A.铁锈的主要成分是氧化铁,与盐酸反应生成的是氯化铁,正确的化学方程式为Fe2O3+6HCl═2FeCl3+3H2O,故错误;
B.空气中的二氧化碳能与水反应生成碳酸,所以正常雨水的pH约为5.6的原因:CO2+H2O═H2CO3,故正确;
C.二氧化碳不支持燃烧,所以除去CO2中少量的CO不能用点燃的方法,可将混合气体通过足量的灼热氧化铜粉末,反应的化学方程式为CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2,故错误;
D.氧化钙能与水反应生成氢氧化钙,所以不能用氧化钙除去氯化钙溶液中的氯化氢,可以用足量的碳酸钙来除,最后过滤即可,故错误.
故选B.
点评 在解此类题时,首先分析应用的原理,然后再根据方程式的书写规则进行判断.

练习册系列答案
相关题目
18.某人用托盘天平称量5.1克食盐时(1克以下用游码),称后发现砝码放在左盘,食盐放在了右盘.所称食盐的实际质量为( )
| A. | 5.3克 | B. | 4.9克 | C. | 5.0克 | D. | 5.1克 |
12.两种溶液混合后能发生化学反应且反应前后溶液的总质量不会发生变化的是( )
| A. | 氯化钠溶液和稀盐酸 | B. | 碳酸钠溶液和稀盐酸 | ||
| C. | 氢氧化钾溶液和稀硫酸 | D. | 石灰石和稀盐酸 |
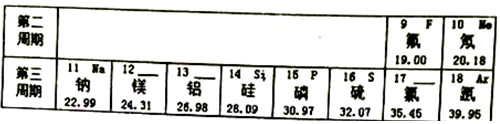
16.对事物进行分类是科学研究的一种重要方法.按所给的标准对事物分类,能分成三类的一组是( )
| A. | 按生物类别区分鲫鱼、金鱼、鲸鱼、娃娃鱼 | |
| B. | 按元素性质区分铁、碳、硫、磷 | |
| C. | 按生态系统的成分区分空气、玉米、蚯蚓、蝗虫 | |
| D. | 按导电性区分塑料、铜丝、橡胶、不锈钢 |
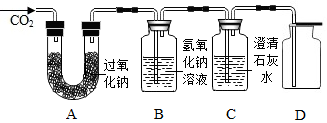 小柯同学在科学课上学习了氧气的实验室制法后,想用其他方法制取氧气.他请教老师后,决定用二氧化碳和过氧化钠反应来制取氧气,该反应原理为:2Na2O2+2CO2=2Na2CO3+O2,其实验装置如图所示:
小柯同学在科学课上学习了氧气的实验室制法后,想用其他方法制取氧气.他请教老师后,决定用二氧化碳和过氧化钠反应来制取氧气,该反应原理为:2Na2O2+2CO2=2Na2CO3+O2,其实验装置如图所示: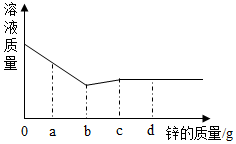 向一定量硝酸银、硝酸镁和硝酸铜的混合溶液中加入一定量的锌,溶液的质量与加入锌的质量的变化关系如图所示.请回答下列问题
向一定量硝酸银、硝酸镁和硝酸铜的混合溶液中加入一定量的锌,溶液的质量与加入锌的质量的变化关系如图所示.请回答下列问题