题目内容
3.将干燥的氯酸钾与二氧化锰混合固体8g放到大试管中加热,反应完全后,冷却到反应前的温度,称量得剩余固体的质量为5.6g.求原混合物中二氧化锰的质量分数是多少?(保留一位小数)分析 加热氯酸钾和二氧化锰的混合物,氯酸钾受热分解生成氯化钾和氧气,二氧化锰在变化过程中为催化剂,反应前后质量和化学性质都不变;利用质量守恒定律,由反应前后固体物质的质量差,可求得放出气体氧气的质量;根据反应的化学方程式,利用生成氧气的质量可计算原混合物中氯酸钾的质量;根据反应后二氧化锰的质量不变可计算其质量分数.
解答 解:利用质量守恒定律,由反应前后固体物质的质量差待反应至不再有气体生成后,制取氧气的质量=8g-5.6g=2.4g
设完全反应时消耗氯酸钾的质量为x
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 96
x 2.4g
$\frac{245}{x}$=$\frac{96}{2.4g}$
x=6.125g
二氧化锰在剩余固体中的质量分数=$\frac{8g-6.125g}{8g}$×100%=23.4%.
给答案为:23.4%.
点评 本题主要考查学生运用化学方程式进行计算的能力,要按照步骤认真完成,此题难度较小.

练习册系列答案
相关题目
14.已知央视3.15晚会曝光,少数不法厂家向液化石油中掺入了二甲醚(C2H6O),二甲醚会对液化气罐的配件造成腐蚀,存在安全隐患.下列关于二甲醚的说法正确的是( )
| A. | 属于氧化物 | |
| B. | 每个分子中含有8个原子 | |
| C. | 二甲醚有2个碳原子6个氢原子和一个氧原子组成 | |
| D. | 它是由碳、氢、氧三种元素组成的 |
11.如图所示的实验操作正确的是( )
| A. | 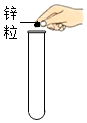 取用固体药品 | B. |  闻气体气味 | C. | 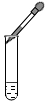 滴加液体 | D. | 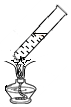 加热液体 |
18.实验室利用高锰酸钾制取氧气,下列有关操作分析不正确的是( )
| A. | 实验前先检查装置的气密性,以防漏气 | |
| B. | 装入药品后,在试管口塞一团棉花,以防加热时高锰酸钾粉末进入导管 | |
| C. | 固定试管时,试管口要略向下倾斜,以防冷凝水回流炸裂试管 | |
| D. | 反应结束时先停止加热,再将导管移出水面,以防水槽中的水倒吸炸裂试管 |
7.A元素的核电荷数为z,Am+和Bn-具有相同的核外电子排列,则B元素核电荷数用z,m,n来表示应为( )
| A. | z+n-m | B. | z-m-n | C. | z+m-n | D. | z+m+n |
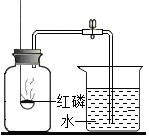 为测定空气里氧气的含量,甲、乙、丙三个小同学用如图所示的装置分别进行了实验探究.
为测定空气里氧气的含量,甲、乙、丙三个小同学用如图所示的装置分别进行了实验探究.