题目内容
工业炼铁是把铁矿石和焦炭等原料一起加入高炉,在高温下通入空气进行一系列反应把铁还原出来.
(1)赤铁矿(主要成分为Fe2O3)在高炉里反应生成单质铁的化学方程式是:
(2)计算:
①Fe2O3的相对分子质量是:
②1000t含氧化铁80%的赤铁矿中,含氧化铁的质量是 t;
③上述赤铁矿理论上可炼得含铁96%的生铁 t.(精确到0.1t)
(1)赤铁矿(主要成分为Fe2O3)在高炉里反应生成单质铁的化学方程式是:
(2)计算:
①Fe2O3的相对分子质量是:
②1000t含氧化铁80%的赤铁矿中,含氧化铁的质量是
③上述赤铁矿理论上可炼得含铁96%的生铁
考点:铁的冶炼,含杂质物质的化学反应的有关计算,相对分子质量的概念及其计算
专题:金属与金属材料
分析:(1)根据赤铁矿的主要成分为氧化铁,则CO和氧化铁反应生成铁和二氧化碳来书写化学反应方程式;
(2)①根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答;
②根据矿石的质量和氧化铁的质量分数计算矿石中氧化铁的质量即可;
③由氧化铁的质量、生铁中铁的质量分数,根据赤铁矿炼铁的化学方程式可以列式计算出炼出生铁的质量.
(2)①根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答;
②根据矿石的质量和氧化铁的质量分数计算矿石中氧化铁的质量即可;
③由氧化铁的质量、生铁中铁的质量分数,根据赤铁矿炼铁的化学方程式可以列式计算出炼出生铁的质量.
解答:解:(1)根据氧化铁和CO反应生成二氧化碳和铁,则反应的化学方程式为Fe2O3+3CO
3CO2+2Fe;
(2)①Fe2O3的相对分子质量是56×2+16×3=160;
②1000t含氧化铁80%的赤铁矿中,其氧化铁的质量是1000t×80%=800t;
③设理论上可炼出含铁96%的生铁质量为x.
Fe2O3+3CO
2Fe+3CO2
160 112
800t 96%x
=
x=583.3t
答:上述赤铁矿理论上可炼得含铁96%的生铁583.3t.
故答案为:(1)Fe2O3+3CO
2Fe+3CO2;
(2)①160;
②800;
③583.3.
| ||
(2)①Fe2O3的相对分子质量是56×2+16×3=160;
②1000t含氧化铁80%的赤铁矿中,其氧化铁的质量是1000t×80%=800t;
③设理论上可炼出含铁96%的生铁质量为x.
Fe2O3+3CO
| ||
160 112
800t 96%x
| 160 |
| 112 |
| 800t |
| 96%x |
x=583.3t
答:上述赤铁矿理论上可炼得含铁96%的生铁583.3t.
故答案为:(1)Fe2O3+3CO
| ||
(2)①160;
②800;
③583.3.
点评:本题考查利用化学反应方程式的计算,注意代入方程式计算的数据为纯物质的质量,学生应学会利用质量分数来计算纯物质的质量.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列汉沽民间制作,其中属于化学变化的是( )
| A、民间绣十字绣 |
| B、版画厂木刻 |
| C、盐场晒盐 |
| D、玫瑰香葡萄酒 |
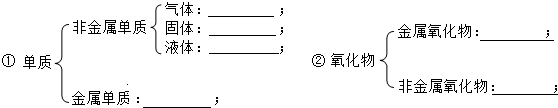
 .请回答下列问题:
.请回答下列问题: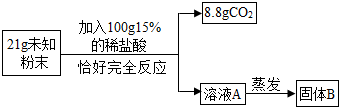
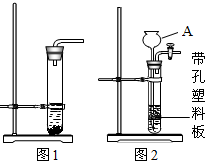 实验室常用石灰石与稀盐酸制取C02,某同学设计了两种制取CO2的部分装置(如图).
实验室常用石灰石与稀盐酸制取C02,某同学设计了两种制取CO2的部分装置(如图).