题目内容
工业上常用电解NaCl溶液的方法来制取NaOH、Cl2和H2,反应的化学方程式为:2NaCl+2H2O
2NaOH+H2↑+Cl2↑.现取NaCl溶液180g进行电解,当NaCl完全反应时,生成0.8gH2.请计算NaCl溶液中溶质的质量分数.
| ||
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据电解NaCl的方程式,由已知反应生成氢气的质量,根据化学方程式可以计算氯化钠的质量,再计算出NaCl溶液中溶质的质量分数.
解答:解:设NaCl溶液中溶质的质量为x,
2NaCl+2H2O
2NaOH+H2↑+Cl2↑,
117 2
x 0.8g
=
解得:x=46.8g
NaCl溶液中溶质的质量分数是:
×100%=26%.
答:NaCl溶液中溶质的质量分数是26%.
2NaCl+2H2O
| ||
117 2
x 0.8g
| 117 |
| 2 |
| x |
| 0.8g |
NaCl溶液中溶质的质量分数是:
| 46.8g |
| 180g |
答:NaCl溶液中溶质的质量分数是26%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,比较简单,只要细心计算即可.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中错误的是( )
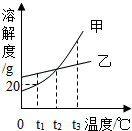

| A、t1℃时,50g甲的饱和溶液中溶解了10g的甲 |
| B、将t2℃时的甲、乙两种物质的饱和溶液升温至t3℃(溶剂的量不变),两种溶液中溶质的质量分数相等 |
| C、t2℃时,要使接近饱和的乙溶液达到饱和状态,可以用蒸发溶剂的方法 |
| D、甲物质的饱和溶液中含有少量乙,可采用降温结晶的方法分离提纯 |
下列图示中的液体物质,可以看作纯净物的是( )
A、 河、湖水 |
B、 蒸馏水 |
C、 灌南汤沟酒 |
D、 自来水 |
下列化学用语的书写或理解错误的是( )
| A、熟石灰的化学式:CaOH | ||
B、过氧乙酸结构式: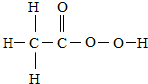 ,其化学式为:C2H4O3 ,其化学式为:C2H4O3 | ||
| C、3个亚铁离子:3Fe2+ | ||
D、漂白精有效成份次氯酸钠(Na
|
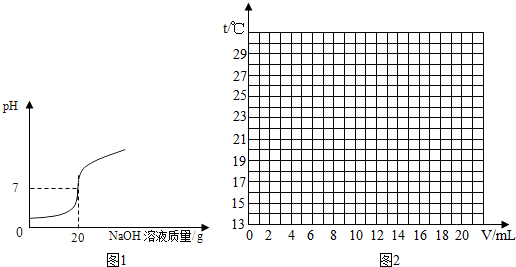
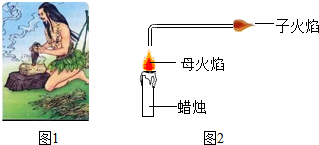 回答问题:
回答问题: