题目内容
5.双氧水(H2O2)既是工业上重要的绿色氧化剂,又是常用的医用消毒剂.(1)小华配制了10%的双氧水500g,则500g溶液中溶质为50克,溶剂为450克.
(2)若要配制质量分数为4%的双氧水,需要加入水的质量为750克.
分析 (1)根据溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%进行计算;
(2)溶液稀释前后,溶质的质量不变.
解答 解:(1)500g溶液中溶质的质量为:=50g.水的质量为500g-50g=450g;
(2)设需要水的质量为x,则
500g×10%=(500g+x)×4%
x=750g.
故答案为:
(1)50;450;(2)750.
点评 根据化学反应方程式的计算的审题是非常关键的,一般是抓住“三找”;即一找化学反应方程式,二找已知量和未知量x,三找用到的相对质量关系,同时注意解题步骤和格式.

练习册系列答案
相关题目
15.下列实验基本操作正确的是( )
| A. |  视线背着刻度量取液体 | B. |  招气法闻气体气味 | ||
| C. |  过滤 | D. |  用滴管反复挤压取液体 |
16.下列物质由离子构成的是( )
| A. | 二氧化碳 | B. | 氯化钠 | C. | 金属铝 | D. | 氧气 |
20.如图化学实验操作,正确的是( )
| A. |  倾倒液体 | B. |  装入固体粉末 | C. |  加热液体 | D. |  读取液体体积 |
10.下列实验现象叙述错误的是( )
| A. | 蜡烛在氧气中燃烧火焰明亮,发出白光 | |
| B. | 铁丝在氧气中燃烧火星四射 | |
| C. | 木炭在氧气中燃烧发出淡蓝色的火焰 | |
| D. | 磷在空气中燃烧放出大量白烟 |
3.下列说法正确的是( )
| A. | 氯化钠是由氯离子和钠离子构成的 | B. | 氯离子的质子数比电子数多1 | ||
| C. | 水银是由水银分子构成的 | D. | 镁原子比镁离子多1个电子 |
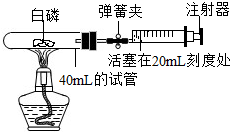 为测定空气中氧气的含量,某兴趣小组的同学选用了40mL的试管作反应容器(如图)和量程体积足够大且润滑效果很好的针筒注射器,将足量的白磷放入试管后,用橡皮塞塞紧试管,并夹紧弹簧夹.用酒精灯加热白磷,燃烧结束后,等到试管冷却后松开弹簧夹,观察现象.
为测定空气中氧气的含量,某兴趣小组的同学选用了40mL的试管作反应容器(如图)和量程体积足够大且润滑效果很好的针筒注射器,将足量的白磷放入试管后,用橡皮塞塞紧试管,并夹紧弹簧夹.用酒精灯加热白磷,燃烧结束后,等到试管冷却后松开弹簧夹,观察现象.