题目内容
10.下列图象能正确反映其对应的实验操作的是( )| A. |  常温下向pH=10的NaOH溶液中不断加入水稀释 | |
| B. |  向等质量的Mg和MgO中分别加入足量等浓度的稀硫酸 | |
| C. | 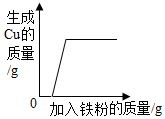 向一定量的Zn(NO3)2和Cu(NO3)2的混合溶液中不断加入铁粉 | |
| D. | 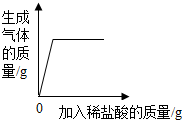 向一定量的部分变质的氢氧化钠溶液中滴加足量的稀盐酸 |
分析 A、根据碱性溶液稀释pH减小解答;
B、根据镁和氧化镁与硫酸的反应解答;
C、根据金属活动性顺序的意义解答;
D、根据部分变质的氢氧化钠溶液中含有氢氧化钠和碳酸钠解答.
解答 解:
A、常温下向pH=10的NaOH溶液中不断加入水稀释,碱性减弱,pH减小,但是不会小于等于7,故A错误;
B、向等质量的Mg和MgO中分别加入足量等浓度的稀硫酸,则镁和氧化镁全部反应,由于等质量的氧化镁中镁元素的质量小于镁中镁元素的质量,故氧化镁生成的硫酸镁的质量小于镁生成的硫酸镁,故B正确;
C、向一定量的Zn(NO3)2和Cu(NO3)2的混合溶液中不断加入铁粉,铁只与硝酸铜开始反应,当硝酸铜反应完毕,铜粉的质量不再改变,故C错误;
D、部分变质的氢氧化钠溶液中含有氢氧化钠和碳酸钠,加入一定量的盐酸,则盐酸首先与氢氧化钠反应,二氧化碳的质量不会从0开始,故D错误.
故选B.
点评 本题考查的是化学反应与图象的关系,完成此题,可以依据已有的化学知识结合图象进行.

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
5.下列4个图象中,能正确反映变化关系的是( )
| A | B | C | D |
 |  |  |  |
| 将一瓶浓硫酸露置于空气中 | 向一定质量的稀硫酸中加入锌片 | 加热一定质量的高锰酸钾固体 | 向一定质量的氯化镁和稀盐酸的混合溶液中逐滴加入氢氧化钠溶液 |
| A. | A | B. | B | C. | C | D. | D |
15. 向一定量的碳酸氢钠和氯化钠的混合溶液中加入稀盐酸溶液至过量,某变量 y随x的变化趋势如图所示.若x表示稀盐酸的质量,则y表示的含义是( )
向一定量的碳酸氢钠和氯化钠的混合溶液中加入稀盐酸溶液至过量,某变量 y随x的变化趋势如图所示.若x表示稀盐酸的质量,则y表示的含义是( )
 向一定量的碳酸氢钠和氯化钠的混合溶液中加入稀盐酸溶液至过量,某变量 y随x的变化趋势如图所示.若x表示稀盐酸的质量,则y表示的含义是( )
向一定量的碳酸氢钠和氯化钠的混合溶液中加入稀盐酸溶液至过量,某变量 y随x的变化趋势如图所示.若x表示稀盐酸的质量,则y表示的含义是( )| A. | 氯化钠的质量 | B. | 溶液的总质量 | ||
| C. | 二氧化碳的质量 | D. | 溶液中钠元素的质量 |
19.下列方法中不能证明空气中有水汽的是( )
| A. | 打开空调时会从空调中涌出雾气 | |
| B. | 寒冷的冬天,戴眼镜的同学从室外走进教室,感到镜片模糊 | |
| C. | 用水壶烧开水,离壶口稍远处有水雾 | |
| D. | 炎热的夏天,人从空调房走到外面时,皮肤上会有潮湿的感觉 |
 实验室利用下列装置制取并收集O2(试管中的棉花根据反应的需要选择是否添加).
实验室利用下列装置制取并收集O2(试管中的棉花根据反应的需要选择是否添加).