题目内容
7.铜和氧化铜的混合物9g,与氢气充分反应后,得到固体物质8g.则原混合物中铜元素的质量分数为( )| A. | 88.9% | B. | 80.0% | C. | 11.1% | D. | 61.5% |
分析 氢气与氧化铜在加热条件下反应生成铜和水,铜和氧化铜的混合物9g,与氢气充分反应后,得到固体物质8g为铜,由质量守恒定律,原混合物中铜元素的质量为8g,据此进行分析判断.
解答 解:氢气与氧化铜在加热条件下反应生成铜和水,铜和氧化铜的混合物9g,与氢气充分反应后,得到固体物质8g为铜,由质量守恒定律,反应前后元素的质量不变,则原混合物中铜元素的质量为8g,则原混合物中铜元素的质量分数为$\frac{8g}{9g}×$100%≈88.9%.
故选:A.
点评 本题难度不大,掌握质量守恒定律、混合物元素质量分数的计算方法是正确解答本题的关键.

练习册系列答案
相关题目
15.某食品厂加工生产的将有中氯化钠的质量分数为15%~18%,该厂日产酱油15t,则该厂每月(按30天计)消耗氯化钠的质量至少为( )
| A. | 67.5t | B. | 13.80t | C. | 73.75t | D. | 22.5t |
2.四位同学在一次小组讨论中,分别发表了各自的观点,其中正确的是( )
| A. | 能使紫色石蕊试液变红的溶液呈酸性 | |
| B. | 能使酚酞试液变红的物质就是碱 | |
| C. | 要鉴别水中是否含有氯离子,可加入AgNO3溶液,观察是否产生白色沉淀 | |
| D. | 能与BaCl2溶液反应产生沉淀的物质就是硫酸 |
11.下列关说法正确的是( )
| A. | 食物的腐败、铁制品的生锈是缓慢氧化,所以缓慢氧化都是有害的 | |
| B. | 工业上采用分离液态空气制取氧气,是利用氮气的沸点比氧气的沸点低 | |
| C. | 用燃着的木条伸入某无色无味的气体中,发现木条熄灭,则该气体是二氧化碳 | |
| D. | 分子和原子的区别是分子可分,原子不可分 |
9.生活中一些物质pH如图所示,下列有关说法正确的( )
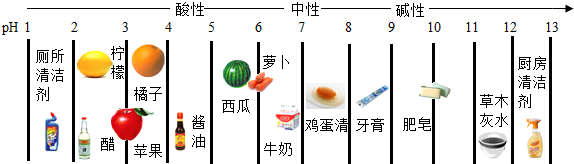

| A. | 草木灰水显碱性农民可把它和碳铵混合一起用 | |
| B. | 胃酸过多的人不宜多吃柠檬橘子 | |
| C. | 为增强洗涤效果可将厕所清洁剂和厨房清洁剂混合使用 | |
| D. | 食醋可使石蕊溶液变蓝也可除水垢 |
