题目内容
7.如图为实验室中常用的几种装置,请回答下列问题: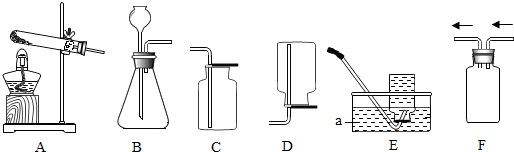
(1)仪器a名称是水槽.
(2)实验室用加热高锰酸钾制取氧气的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,所选用的发生装置是A(填序号,下同),所选用的收集装置是C或E,若用F装置进行“排空气法”收集CO2,请把图中的“导气管”补画完整.
(3)实验室用稀盐酸和大理石制取二氧化碳时选用的制取装置是BC,检验集气瓶中CO2是否集满的方法是将燃着的木条放在集气瓶口,木条熄灭,证明二氧化碳已经集满;
(4)某同学用浓盐酸和大理石制取的CO2能使紫色石蕊溶液变红,对这一现象的合理解释有②③(填序号).
①产生的CO2直接使石蕊试液变红
②产生的CO2与水反应生成H2CO3,使石蕊溶液变红
③浓盐酸挥发出的氯化氢溶于水使石蕊溶液变红.
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,氧气密度比空气大,不易溶于水进行分析;
(3)根据实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,二氧化碳密度比空气大,不具有助燃性进行分析;
(4)根据浓盐酸和二氧化碳的性质分析烧杯中紫色石蕊溶液变红色的原因.
解答 解:(1)通过分析题中所指仪器的作用可知,a是水槽;
(2)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,氧气密度比空气大,不易溶于水,所选用的发生装置是A,所选用的收集装置是C或E,用F装置进行“排空气法”收集CO2的装置图是
;
(3)实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,所以制取二氧化碳时选用的制取装置是BC,二氧化碳密度比空气大,不具有助燃性,所以检验集气瓶中CO2是否集满的方法是:将燃着的木条放在集气瓶口,木条熄灭,证明二氧化碳已经集满;
(4)二氧化碳和水反应生成的碳酸具有酸性,氯化氢溶于水形成的盐酸具有酸性,紫色石蕊遇酸变红色,故选:②③.
故答案为:(1)水槽;
(2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,A,C或E, ;
;
(3)BC,将燃着的木条放在集气瓶口,木条熄灭,证明二氧化碳已经集满;
(4)②③.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

 备战中考寒假系列答案
备战中考寒假系列答案| A. |  灭火焰 | B. |  闻气味 | C. |  读体积 | D. |  测水温 |
| A. | 向某固体中加入稀盐酸有气泡产生,可证明该物质中一定含有CO32- | |
| B. | 常温下可用Fe与AgCl反应制取Ag | |
| C. | 可用过量的Cu(OH)2除去CuSO4溶液中少量的H2SO4 | |
| D. | 将Fe(OH)3加入到滴有酚酞试液的蒸馏水中,溶液显红色 |
 甲、乙、丙、丁四种物质的相互反应关系如图所示(“一”表示相连的物质间能发生反应)下列符合对应反应关系的选项是( )
甲、乙、丙、丁四种物质的相互反应关系如图所示(“一”表示相连的物质间能发生反应)下列符合对应反应关系的选项是( ) | 选项 | A | B | C | D | |
| 物 | 甲 | BaCl2 | CO2 | H2 | Fe |
| 乙 | Na2CO3 | NaOH | O2 | HCl | |
| 质 | 丙 | H2SO4 | CaCl2 | CuO | CuSO4 |
| 丁 | Ca(OH)2 | AgNO3 | CO | NaOH | |
| A. | A | B. | B | C. | C | D. | D |
| A. | 百炼成钢 | B. | 花香四溢 | C. | 滴水成冰 | D. | 扬汤止沸 |
| A. | 浓硫酸 | B. | 浓盐酸 | C. | 氢氧化钠固体 | D. | 碳酸钙 |
| A. | 有机物:甲烷、乙醇、葡萄糖 | |
| B. | 复合肥料:KNO3、K2CO3、(NH4)2HPO4 | |
| C. | 混合物:煤、石油、冰水共存物 | |
| D. | 三大合成材料:合金、合成纤维、合成橡胶 |




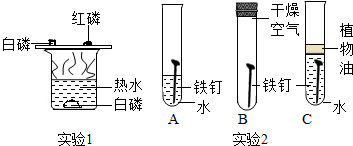 化学式一门以实验为基础的科学,根据下列实验回答有关问题:
化学式一门以实验为基础的科学,根据下列实验回答有关问题: