题目内容
17. 化学式一门以实验为基础的科学,根据下列实验回答有关问题:
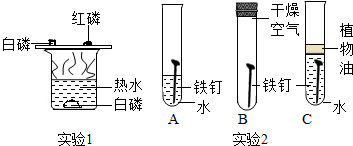
化学式一门以实验为基础的科学,根据下列实验回答有关问题:(1)实验1:观察到铜片上的白磷燃烧而红磷不燃烧(或铜片上的白磷燃烧,热水中的白磷没有燃烧),可得出可燃物的一个条件为:温度要达到着火点(或燃烧需要氧气).
(2)实验2:对比铁钉表面的不同现象,可得知防止铁生锈的原理是隔绝氧气或水分.
分析 (1)物质燃烧需同时具备三个条件,缺一不可:(1)物质具有可燃性;(2)可燃物与氧气接触;(3)温度达到可燃物的着火点.
(2)根据植物油可以隔绝氧气、干燥的空气不含水分,分析防止铁生锈的原理.
解答 解:(1)白磷的着火点是40℃,80℃的热水可以达到其着火点,而红磷的着火点高,热水不能使其达到着火点;根据铜片上的白磷燃烧而红磷不燃烧的事实,可得出可燃物燃烧的其中一个条件是温度要达到着火点.铜片上的白磷燃烧,热水中的白磷没有燃烧,说明燃烧需要氧气;故填:铜片上的白磷燃烧而红磷不燃烧(或铜片上的白磷燃烧,热水中的白磷没有燃烧);温度要达到着火点(或燃烧需要氧气);
(2)蒸馏水被植物油隔绝空气的铁钉不生锈,干燥空气中的铁钉不生锈,而蒸馏水中的铁钉生锈,说明铁生锈的条件是:与氧气和水接触,则防止铁生锈的原理是隔绝氧气或水分.
故答案为:隔绝氧气或水分.
点评 本题难度不大,掌握燃烧的条件、铁生锈的条件与防止铁生锈的原理是正确解答本题的关键.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
5.物质的性质决定用途.下列物质的用途中利用其物理性质的是( )
| A. | 液氮作冷冻剂 | B. | 稀盐酸作除锈剂 | C. | 生石灰作干燥剂 | D. | 碳酸钙作补钙剂 |
2.元素化合价发生改变的反应都是氧化还原反应.例如:2$\stackrel{0}{Fe}$+3$\stackrel{0}{C{l}_{2}}$$\frac{\underline{\;点燃\;}}{\;}$2$\stackrel{+3}{Fe}$$\stackrel{-1}{C{l}_{2}}$,反应前后,铁元素和氯元素的化合价发生了改变,该反应是氧化还原反应.下列反应不属于氧化还原反应的是( )
| A. | C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO | B. | HCl+NaOH═H2O+NaCl | ||
| C. | Zn+H2SO4═ZnSO4+H2↑ | D. | 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ |
6.推理是化学学习中常用的思维方法.下列推断不正确的是( )
| A. | 碱溶液一定呈碱性,呈碱性的溶液不一定是碱溶液 | |
| B. | 置换反应一定有单质生成,有单质生成的反应不一定是置换反应 | |
| C. | 氧化物中一定含氧元素,含氧元素的化合物一定是氧化物 | |
| D. | 单质是只含一种元素的纯净物,含有一种元素的纯净物一定是单质 |
7.下列物质放入水中,能形成溶液的是( )
| A. | 食盐 | B. | 石灰石 | C. | 面粉 | D. | 植物油 |
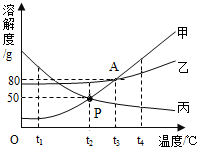 如图为甲、乙、丙三种物质的溶解度曲线.回答下列问题:
如图为甲、乙、丙三种物质的溶解度曲线.回答下列问题: A、B、C、D是初中化学常见的物质,各物质之间的相互转化的关系如图所示(部分反应物、生成物及条件略去).已知:四种物质均含有铜元素,且铜在化合物中均为+2价;A为单质,C溶液呈蓝色;D为不溶于水的蓝色固体.
A、B、C、D是初中化学常见的物质,各物质之间的相互转化的关系如图所示(部分反应物、生成物及条件略去).已知:四种物质均含有铜元素,且铜在化合物中均为+2价;A为单质,C溶液呈蓝色;D为不溶于水的蓝色固体.