题目内容
8.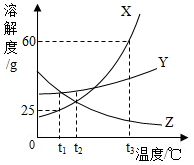 如图所示为X、Y、Z三种固体物质(不含结晶水)的溶解度曲线,请回答下列问题:
如图所示为X、Y、Z三种固体物质(不含结晶水)的溶解度曲线,请回答下列问题:(1)X中含有少量Y,应采用降温结晶的方法提纯X.
(2)t2℃时,三种物质的溶解度的大小关系是Y>X=Z.
(3)t3℃时,溶质质量分数为25%的X溶液降温到t1℃,所得溶液中溶质质量分数是20%.
(4)t3℃时,等质量X、Y、Z的饱和溶液分别降温到t1℃,溶液质量没有变化的是Z.
分析 根据题目信息和溶解度曲线可知:X、Y两种固体物质的溶解度,都是随温度升高而增大,而Z的溶解度随温度的升高而减少;X中含有少量Y,应采用降温结晶的方法提纯X;t2℃时,三种物质的溶解度的大小关系是:Y>X=Z;t3℃时,溶质质量分数为25%的X溶液降温到t1℃,有晶体析出,因为降温后溶液是饱和的,所得溶液中溶质质量分数是20%,;t3℃时,等质量X、Y、Z的饱和溶液分别降温到t1℃,溶液质量没有变化的是:Z.
解答 解:(1)X中含有少量Y,应采用降温结晶的方法提纯X,因为X的溶解度随温度的升高变化比Y大,故答案为:降温结晶;
(2)由溶解度曲线可知:t2℃时,三种物质的溶解度的大小关系是:Y>X=Z;故答案为:Y>X=Z;
(3)t3℃时,溶质质量分数为25%的X溶液降温到t1℃,降温后所得饱和溶液的质量分数=$\frac{25g}{125g}×100%$=20%,25%>20%,所以降温后有晶体析出,溶液是饱和的;故答案为:20%;
(4)t3℃时,等质量X、Y、Z的饱和溶液分别降温到t1℃,溶液质量没有变化的是:Z,因为Z的溶解度随温度的升高而减少,故答案为:
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.

练习册系列答案
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
19.某物质在点燃的条件下发生反应,生成物和反应物共四种,它们的微观示意图和反应前后的质量如表所示.
(1)由 构成的物质中
构成的物质中 所代表的元素的化合价为-2;
所代表的元素的化合价为-2;
(2)表中的四种物质中,属于氧化物的是H2O和SO2(填化学式);
(3)上述反应的化学方程式为2H2S+3O2$\frac{\underline{\;点燃\;}}{\;}$2H2O+2SO2;
(4)一位同学在计算x、y和z数值的过程中,列出了以下等式,其中正确的是AD(填字母序号).
A.x+y+z=169 B.y+z=168
C.(100-x):z=32:64 D.(100-x):(y-1)=8:3.
| 物质序号 | 甲 | 乙 | 丙 | 丁 |  |
| 微观 示意图 |  |  |  |  | |
| 反应前质量/g | 68 | 100 | 1 | 0 | |
| 反应后质量/g | 0 | x | y | z |
 构成的物质中
构成的物质中 所代表的元素的化合价为-2;
所代表的元素的化合价为-2;(2)表中的四种物质中,属于氧化物的是H2O和SO2(填化学式);
(3)上述反应的化学方程式为2H2S+3O2$\frac{\underline{\;点燃\;}}{\;}$2H2O+2SO2;
(4)一位同学在计算x、y和z数值的过程中,列出了以下等式,其中正确的是AD(填字母序号).
A.x+y+z=169 B.y+z=168
C.(100-x):z=32:64 D.(100-x):(y-1)=8:3.
3.某纯净物3g在氧气中完全燃烧,生成8.8g二氧化碳和5.4g水.下列说法不正确的是( )
| A. | 该纯净物中含有C、H元素,不含O元素 | |
| B. | 该反应中O2和CO2的质量比为14:11 | |
| C. | 该反应中O2和H2O的分子数之比为7:6 | |
| D. | 该纯净物中C、H原子的个数比为1:4 |
13.下列图象不能正确反映其对应变化关系的是( )
| A. |  向一定质量的硫酸铜和稀硫酸的混合溶液中逐滴加入氢氧化钠溶液 | |
| B. |  向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉 | |
| C. |  用等质量、等溶液的过氧化氢溶液在有无催化剂条件下制氧气 | |
| D. |  一定质量稀盐酸中逐滴加入氢氧化钠溶液 |
20.水是生命之源.下列有关水的叙述正确的是( )
| A. | 用肥皂水可以鉴别软水和硬水 | |
| B. | 为了节约用水,直接用工业污水灌溉农田 | |
| C. | 水中Ca2+、Mg2+增多会导致水中藻类植物大量生长和繁殖 | |
| D. | 水是由氢原子和氧原子组成 |
8.下列排列顺序正确的是( )
| A. | 空气中物质的含量: | B. | 室温时水中溶解度: | ||
| C. | 溶液的pH: | D. | 铁元素的质量分数: |

