题目内容
13.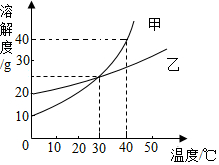 如图是甲、乙两固体物质的溶解度随温度变化的曲线图,据此回答下列问题:
如图是甲、乙两固体物质的溶解度随温度变化的曲线图,据此回答下列问题:(1)40℃时,甲物质溶解度为35 g.
(2)溶解度随温度变化影响比较大的物质是甲.
(3)饱和溶液(填“饱和”或“不饱和”),所得溶液中溶质的质量分数为20%.
分析 由溶解度曲线:可以查出40℃时,甲物质溶解度;可以判断溶解度随温度变化影响比较大的物质;由30℃时乙的溶解度,可以判断100g水中加入30g乙物质能否形成饱和溶液,根据溶解度计算饱和溶液中溶质的质量分数.
解答 解:(1)由甲物质的溶解度随温度变化的曲线图可知,在40℃时,甲物质溶解度为35g.
(2)由甲、乙两固体物质的溶解度随温度变化的曲线图可知,甲的溶解度受温度影响较大,故溶解度随温度变化影响比较大的物质是甲.
(3)30℃时,乙的溶解度为25g,故向100g水中加入30g乙物质,充分溶解后,只能溶解25g,故所得溶液是饱和溶液;所得溶液中溶质的质量分数为:$\frac{25g}{100g+25g}×100%$=20%.
答案:(1)35;(2)甲;(3)饱和,20%.
点评 本题难度不大,主要考查了固体溶解度曲线所表示的意义,通过本题可以加强学生对固体溶解度的理解,培养学生应用知识解决问题的能力.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
18.某化学兴趣小组利用如图所示装置进行“过氧化钠(Na2O2)与CO2反应”等实验探究活动.装置气密性良好,所用试剂均足量.装置内的空气对实验的影响可以忽略.实验所用过氧化钠药品中所含杂质不参加化学反应.已知:(1).碱石灰是由固体NaOH和CaO组成的混合物.
(2).NaHCO3不与CO2反应.饱和NaHCO3溶液可吸收HCl气体.
(3).过氧化钠是一种淡黄色粉末状固体,Na2O2能与CO2反应:2Na2O2+2CO2═2Na2CO3+O2,也能与H2O反应:2Na2O2+2H2O═4NaOH+O2↑.
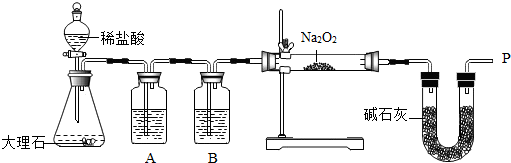
主要探究过程记录如下:
有关数据记录如下:玻璃管中过氧化钠药品的质量为m,操作Ⅱ再次测得玻璃管内固体质量n.
请回答下列问题:
(1)锥形瓶中发生反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)若A瓶所装试剂是饱和NaHCO3溶液,则B瓶所装试剂是浓硫酸.
(3)操作Ⅰ空白处记录的实验现象是带火星的木条复燃.
(4)操作Ⅱ“烧杯中无明显现象”说明过氧化钠完全反应.
(5)药品中过氧化钠的质量分数用m和n的代数式表示为$\frac{15600(n-m)}{56m}$%.
(2).NaHCO3不与CO2反应.饱和NaHCO3溶液可吸收HCl气体.
(3).过氧化钠是一种淡黄色粉末状固体,Na2O2能与CO2反应:2Na2O2+2CO2═2Na2CO3+O2,也能与H2O反应:2Na2O2+2H2O═4NaOH+O2↑.

主要探究过程记录如下:
| 实验操作 | 实验现象 |
| Ⅰ.打开分液漏斗旋塞,向锥形瓶中注入足量稀盐酸后关闭;一段时间后在导管口P处用带火星的木条检验导出的气体 | 锥形瓶内产生大量气泡 |
| Ⅱ.观察到玻璃管内固体变为白色后,再次测定玻璃管内固体质量;测定固体质量完毕后将固体溶于盛有适量水的烧杯中 | 烧杯中无明显现象 |
请回答下列问题:
(1)锥形瓶中发生反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)若A瓶所装试剂是饱和NaHCO3溶液,则B瓶所装试剂是浓硫酸.
(3)操作Ⅰ空白处记录的实验现象是带火星的木条复燃.
(4)操作Ⅱ“烧杯中无明显现象”说明过氧化钠完全反应.
(5)药品中过氧化钠的质量分数用m和n的代数式表示为$\frac{15600(n-m)}{56m}$%.
5.潜水艇中通常用过氧化钠作供氧剂,其反应原理为2Na2O2+2CO2═O2+2X.下列有关说法正确的是( )
| A. | 该反应为置换反应 | |
| B. | Na2O2中氧元素的化合价为-2价 | |
| C. | X的相对分子质量为116 | |
| D. | 利用该反应可以维持艇内空气成分的相对稳定 |
2.有三瓶无标签的无色溶液,只知道它们分别是稀盐酸、CaCl2溶液和KNO3溶液中的各一种.下列四种溶液中,能将三种无色溶液一次鉴别出来的是( )
| A. | NaCl溶液 | B. | 稀硫酸 | C. | Na2CO3溶液 | D. | AgNO3溶液 |
3.下列实验基本操作正确的是( )
| A. |  倾倒液体 | B. | 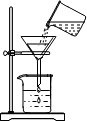 过滤 | C. | 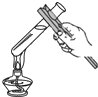 给液体加热 | D. | 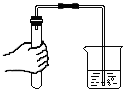 检查装置气密性 |
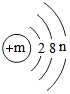 (其中n≠0),若m-n=10,则该粒子对应的常见金属元素有
(其中n≠0),若m-n=10,则该粒子对应的常见金属元素有