题目内容
1.生活中常见的黄铜是铜-锌合金,某同学取20g黄铜样品加入足量的稀硫酸中,待反应完全后过滤,称得不溶物的质量为7g.问:(1)黄铜中锌的质量?
(2)产生氢气的质量?
分析 依据金属活动性顺序的应用可知铜不会与稀硫酸反应而锌可以分析解决;
依据反应的锌的质量可求氢气的质量.
解答 解:(1)由分析可知剩余的不溶物为铜,故锌的质量为20g-7g=13g;
(2)解:设样产生氢气的质量为x
Zn+H2SO4=ZnSO4+H2↑
65 2
13g x
$\frac{65}{13g}=\frac{2}{x}$,
x=0.4g
答:产生氢气的质量是0.4g.
点评 本题主要考查了根据化学方程式的计算,要想解答好这类题目,就要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的物质的质量等知识.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.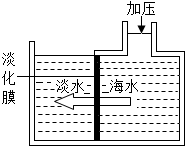 淡化海水可采用膜分离技术(如图),水分子可以透过膜(海水中其他粒子不能透过)进入左侧的池子,从而得到淡水.以下分析中正确的是( )
淡化海水可采用膜分离技术(如图),水分子可以透过膜(海水中其他粒子不能透过)进入左侧的池子,从而得到淡水.以下分析中正确的是( )
 淡化海水可采用膜分离技术(如图),水分子可以透过膜(海水中其他粒子不能透过)进入左侧的池子,从而得到淡水.以下分析中正确的是( )
淡化海水可采用膜分离技术(如图),水分子可以透过膜(海水中其他粒子不能透过)进入左侧的池子,从而得到淡水.以下分析中正确的是( )| A. | 这种膜可用滤纸代替 | B. | 左侧池中的淡水属于混合物 | ||
| C. | 右侧池中溶剂的质量减少 | D. | 右侧池中海水的溶质质量分数不变 |
16.已知某化学肥料是NH4NO3和K2SO4固体的混合物,其中氮元素的质量分数为14%,则混合物中K2SO4的质量分数为( )
| A. | 20% | B. | 25% | C. | 60% | D. | 86% |
13.下列各组离子在水中一定能大量共存的是( )
| A. | H+、Cl-、HCO3- | B. | Ca2+、CO32-、NO3- | C. | NH4+、OH-、NO3- | D. | Na+、Fe2+、SO42- |
18.互为同素异形体的一组物质是( )
| A. | 氧气与液氧 | B. | CO2与CO | C. | 干冰与冰 | D. | 金刚石与石墨 |
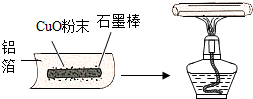 小洋和他的课外兴趣小组对碳还原氧化铜的实验进行了如下创新探究,取一根洁净的石墨棒,置于一张大小适宜的铝箱内,在其表面均匀撒上适量氧化铜粉末,将其包紧,置于酒精灯上加热(如图),几分钟后,冷却,拆开铝箱,发现氧化铜由黑色变为红色.
小洋和他的课外兴趣小组对碳还原氧化铜的实验进行了如下创新探究,取一根洁净的石墨棒,置于一张大小适宜的铝箱内,在其表面均匀撒上适量氧化铜粉末,将其包紧,置于酒精灯上加热(如图),几分钟后,冷却,拆开铝箱,发现氧化铜由黑色变为红色.