题目内容
1.实验室利用如图实验装置进行有关化学实验,回答下列问题: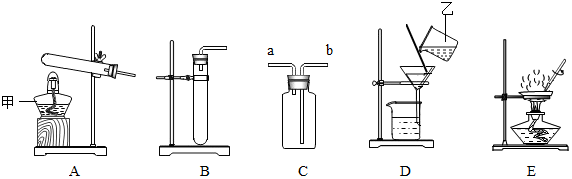
(1)写出图A中仪器名称:甲酒精灯.
(2)实验室用高锰酸钾制取氧气,写出该反应的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.用充满水的装置C收集氧气,则氧气需从a(填“a”或“b”)端通人.
(3)实验室制取二氧化碳的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑,可选用B(填编号)为发生装置.
(4)用上述制取二氧化碳实验后的固液残留物进行过滤、蒸发的操作训练.
①对固液残留物进行过滤,应选择图8中(填标号)装置,过滤时玻璃棒的作用是引流作用;
②取上述少量滤液进行蒸发,析出的固体中一定含有的物质是CaCl2(填化学式).
分析 酒精灯是常用的加热仪器,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.过滤时玻璃棒的作用是:引流作用;取上述少量滤液进行蒸发,析出的固体中一定含有的物质是氯化钙.
解答 解:(1)酒精灯是常用的加热仪器,故答案为:酒精灯;
(2)高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;用充满水的装置C收集氧气,则氧气需从a进入,因为气体的密度比水小;故答案为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;a;
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;B;
(4)过滤时玻璃棒的作用是:引流作用;取上述少量滤液进行蒸发,析出的固体中一定含有的物质是氯化钙;故答案为:①引流作用;②CaCl2;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、过滤和蒸发操作等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
9.下列有关氧气的说法中错误的是( )
| A. | 氧气约占空气总体积的$\frac{1}{5}$ | |
| B. | 氧气能支持燃烧,说明氧气具有可燃性 | |
| C. | 氧气能供给呼吸,它和体内物质反应,释放能量,维持生命活动需要 | |
| D. | 氧气能用排水法收集,说明氧气不易溶于水 |
16.如表为NH4C1、NaC1、KNO3在不同温度下的溶解度,根据表中数据,回答有关问题.
(1)写出NH4C1和NaCl具有相同溶解度的温度范围 (限相邻两个温度之间):10~20℃.
(2)50℃时,50g水中溶解18.5 g的NaCl即成该温度下NaCl的饱和溶液.此温度时,向100g水中加入90g硝酸钾,充分溶解后,得到硝酸钾溶液185.5g.
(3)60℃时,配制硝酸钾溶液的溶质质量分数最大为52.4%.
| 温度/℃ 溶解度/g 溶质 | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 60.2 | 65.6 |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 |
(2)50℃时,50g水中溶解18.5 g的NaCl即成该温度下NaCl的饱和溶液.此温度时,向100g水中加入90g硝酸钾,充分溶解后,得到硝酸钾溶液185.5g.
(3)60℃时,配制硝酸钾溶液的溶质质量分数最大为52.4%.
13.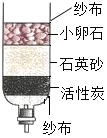 如图是用来净化河水的简易装置,下面对该净水器分析正确的是( )
如图是用来净化河水的简易装置,下面对该净水器分析正确的是( )
 如图是用来净化河水的简易装置,下面对该净水器分析正确的是( )
如图是用来净化河水的简易装置,下面对该净水器分析正确的是( )| A. | 能把硬水软化 | |
| B. | 能杀菌消毒 | |
| C. | 能得到纯净水 | |
| D. | 活性炭主要起吸附异味、色素的作用 |
10.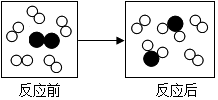 如图是某个化学反应的微观模拟图,不同颜色的小圈代表不同原子,下列关于该化学反应的说法中正确的是( )
如图是某个化学反应的微观模拟图,不同颜色的小圈代表不同原子,下列关于该化学反应的说法中正确的是( )
 如图是某个化学反应的微观模拟图,不同颜色的小圈代表不同原子,下列关于该化学反应的说法中正确的是( )
如图是某个化学反应的微观模拟图,不同颜色的小圈代表不同原子,下列关于该化学反应的说法中正确的是( )| A. | 反应前后原子总数减少 | B. | 反应前后分子总数不变 | ||
| C. | 反应前后元素的种类不变 | D. | 反应前后物质的总质量减少 |
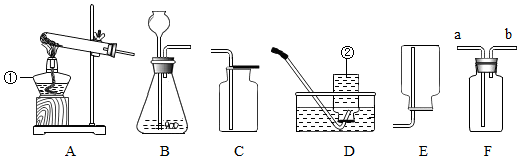

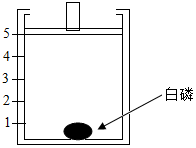 为测定空气中氧气的含量,小华同学打算设计如图所示的实验方案:
为测定空气中氧气的含量,小华同学打算设计如图所示的实验方案: